题目内容
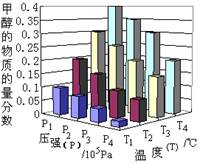
将2molCO2和6molH2充入容积为3L的密闭容器中,在一定温度和压强条件下发生了下列反应:CO2(g)+3H2 (g) CH3OH(g)+H2O(g) ΔH=- 49.0 kJ·mol-1。反应达到平衡时,改变温度(T)和压强(P),反应混合物中CH3OH的“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是
CH3OH(g)+H2O(g) ΔH=- 49.0 kJ·mol-1。反应达到平衡时,改变温度(T)和压强(P),反应混合物中CH3OH的“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是
 CH3OH(g)+H2O(g) ΔH=- 49.0 kJ·mol-1。反应达到平衡时,改变温度(T)和压强(P),反应混合物中CH3OH的“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是
CH3OH(g)+H2O(g) ΔH=- 49.0 kJ·mol-1。反应达到平衡时,改变温度(T)和压强(P),反应混合物中CH3OH的“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是
| A.P3>P2T3>T2 |
| B.P2>P4T4>T2 |
| C.P1>P3T3>T1 |
| D.P1>P4T2>T3 |
D
该反应是体积减小的、放热的可逆反应,所以温度越低或压强越大,生成物甲醇的含量越多,所以根据图像可知,温度是T1>T2>T>T3,压强是P1>P2>P3>P4 ,答案选D。

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
 2AB(g),达到平衡的标志的是( )
2AB(g),达到平衡的标志的是( ) 2C2 (g)+2D(g),可以作为反应达到平衡的标志是(C )
2C2 (g)+2D(g),可以作为反应达到平衡的标志是(C ) 3Z(气)+2W(气),在某时刻测定出的下列各生成物的浓度,一定不正确的是
3Z(气)+2W(气),在某时刻测定出的下列各生成物的浓度,一定不正确的是
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如下表:
 PCl5(g),达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
PCl5(g),达平衡时,PCl5为0.4mol,如果此时移走1.0 molPCl3和0.50 molCl2,在相同温度下再达平衡时PCl5的物质的量是( ) B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。 R(g)+S(g)在恒温下已达到平衡
R(g)+S(g)在恒温下已达到平衡 CH3OH(g)
CH3OH(g)