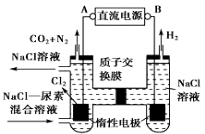
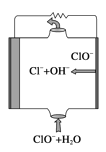
��Ŀ����
����Ŀ�����������ҹ�����̼���о�����ش��չ���绡���ϳ�̼���ܣ������д������ʡ�̼������������̼���������������������ᴿ���䷴Ӧ�Ļ�ѧ����ʽΪ��
______C+______K2Cr2O7+______H2SO4(ϡ) �� _____CO2��+_____K2SO4+ ______ Cr2(SO4)3+ ______H2O
��1����ɲ���ƽ������Ӧ�Ļ�ѧ����ʽ
��2���˷�Ӧ����������________������������__________��
��3�������Ӧ�е���ת�Ƶķ������Ŀ��
��4��������Ӧ������11g�������ʣ���ת�Ƶ��ӵ���ĿΪ___________��
���𰸡���1��3C+2K2Cr2O7+8H2SO4(ϡ) =3CO2��+2K2SO4+2Cr2(SO4)3+8H2O
��2��K2Cr2O7 CO2
��3��![]()
��4��NA
��������
�����������1�����ݵ�ʧ�����غ㣬��Ӧ�Ļ�ѧ����ʽΪ3C+2K2Cr2O7+8H2SO4(ϡ) = 3CO2�� + 2K2SO4 + 2Cr2(SO4)3 + 8H2O��
��2��K2Cr2O7��CrԪ�ػ��ϼ۽��ͣ��˷�Ӧ����������K2Cr2O7��̼Ԫ�ػ��ϼ����߱�����ΪCO2������������CO2��
��3��![]()
��4��������Ӧ������11g�������ʣ���ת�Ƶ��ӵ���Ŀ![]() = NA��
= NA��

 ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д�����Ŀ��700��ʱ��H2��g����CO2��g��![]() H2O��g����CO��g�������¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��CO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��v(H2O)Ϊ0.025mol/��L��min���������жϲ���ȷ����
H2O��g����CO��g�������¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��CO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��v(H2O)Ϊ0.025mol/��L��min���������жϲ���ȷ����
��ʼŨ�� | �� | �� | �� |
c(H2)/mol/L | 0.10 | 0.20 | 0.20 |
c(CO2)/mol/L | 0.10 | 0.10 | 0.20 |
A��ƽ��ʱ������CO2��ת���ʴ���50��
B������Ӧƽ��ʱ������c��CO2���Ǽ��е�2��
C���¶�����800�棬������Ӧƽ�ⳣ��Ϊ25/16��������ӦΪ���ȷ�Ӧ
D�������������䣬����ʼ���������г���0.10mol/L H2��0.20 mol/L CO2������ƽ��ʱc (CO)���Ҳ�ͬ