题目内容
【题目】在100mL2mol/L的盐酸反应中分别加入等物质的量的金属Na、Mg、Al,充分生成气体的体积均为VL(标准状况下),下列说法正确的是( )
A.反应中,每生成1molH2转移的电子数均为2mol
B.参加反应的金属Na、Mg、Al的物质的量之比为1:2:3
C.镁的物质的量为0.1mol
D.V=2.24
【答案】A,C,D
【解析】A、反应中,每生成1molH2需2mol氢离子得电子,所以转移的电子数均为2mol,A符合题意;
B、Na、Mg、Al均与盐酸反应生成氢气,盐酸不足时,Mg、Al不能与水反应,而Na能与水反应生成氢气,根据氢元素守恒,可知Mg、Al与盐酸反应最多生成氢气为0.1L×2mol/L× ![]() =0.1mol,其体积为0.1mol×22.4L/mol=2.24L,由关系式:2Na~H2,Mg~H2,2Al~3H2,可得生成气体与金属的物质的量关系图为:
=0.1mol,其体积为0.1mol×22.4L/mol=2.24L,由关系式:2Na~H2,Mg~H2,2Al~3H2,可得生成气体与金属的物质的量关系图为: 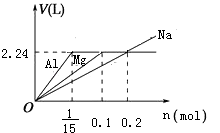 ,反应生成气体的体积均为VL(标准状况下),说明反应生成氢气为2.24L,金属Al、Mg过量,Na恰好完全反应,参加反应的金属Na、Mg、Al的物质的量分别为0.2mol、0.1mol、
,反应生成气体的体积均为VL(标准状况下),说明反应生成氢气为2.24L,金属Al、Mg过量,Na恰好完全反应,参加反应的金属Na、Mg、Al的物质的量分别为0.2mol、0.1mol、 ![]() mol,参加反应的金属Na、Mg、Al的物质的量之比为0.2mol:0.1mol:
mol,参加反应的金属Na、Mg、Al的物质的量之比为0.2mol:0.1mol: ![]() mol=6:3:2,综上分析可知,B不符合题意;
mol=6:3:2,综上分析可知,B不符合题意;
C、由B可知,镁的物质的量为0.1mol,C符合题意;
D、Na、Mg、Al均与盐酸反应生成氢气,盐酸不足时,Mg、Al不能与水反应,而Na能与水反应生成氢气,根据氢元素守恒,可知Mg、Al与盐酸反应最多生成氢气为0.1L×2mol/L× ![]() =0.1mol,其体积为0.1mol×22.4L/mol=2.24L,D符合题意;
=0.1mol,其体积为0.1mol×22.4L/mol=2.24L,D符合题意;
所以答案是:ACD

练习册系列答案
相关题目