题目内容
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
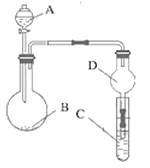
A. 若A为浓盐酸,B为MnO2,C中盛品红试液,则C中溶液褪色
B. 实验仪器D可以起到防止溶液倒吸的作用
C. 若A为浓氨水,B为生石灰,C中盛A1C13溶液,则C中先产生白色沉淀后沉淀又溶解
D. 若A为醋酸,B为贝壳,C中盛有澄清石灰水,则C中溶液不变浑浊
【答案】B
【解析】试题分析:A.若A为浓盐酸,B为MnO2,二者加热生成氯气,把氯气通到紫色石蕊溶液中,氯气与水反应生成HCl和HClO,HCl使紫色石蕊溶液变红,HClO具有漂白性,使溶液褪色,但图中缺少加热装置,错误;B.导气管下端连接球形干燥管时,由于球形干燥管中间部分较粗,盛放的液体的量较多,倒吸的液体靠自身重量回落,因此可以防止液体倒吸,正确;C.若A为浓氨水,B为生石灰,滴入后反应生成氨气,氨气和铝离子反应生成氢氧化铝,但氢氧化铝不溶于氨水,所以C中产生白色沉淀不溶解,错误;D.醋酸与碳酸钙反应生成二氧化碳,然后二氧化碳与石灰水反应生成碳酸钙,则C中溶液变浑浊,错误。

 名校课堂系列答案
名校课堂系列答案【题目】己知A、B、C、D、E、F、G都是周期表中前四周期的元素,他们的原子序数依次增大。其中A原子的L层有2个未成对电子。D是电负性最大的元素,E与F同主族,E的二价阳离子与C的阴离子具有相同的电子层结构。G3+离子3d轨道电子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
⑴A、B、C的第一电离能由小到大的順序为_____________。D的核外有____种运动状态不同的电子。
⑵A的最简单氢化物属于______(填“极性分子”和“非极性分子”)。AH3+离子空间构型是________,其中心原子采取______杂化。
⑶G和M (质子数为25)两元素的部分电离能数据列于下表:
元素 | M | G | |
电离能 (kJmol-1) | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态G2+再失去一个电子难。其原因是____________;
⑷晶体熔点:EC____FC (填“ > ”、“<”或“=”),原因是_______________。
(5)H2S和C元素的一种氢化物(分子式为H2C2)的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
h2s | 187 | 202 | 2.6 |
H2C2 | 272 | 423 | 以任意比互溶 |
h2s和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因___________。
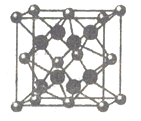
(6)FD2晶胞如图,已知DF核间距为a pm,则该晶体密度ρ=______g㎝-3(用带a、NA的算式表示,不必化简)