题目内容
X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(水及部分产物已略去)。
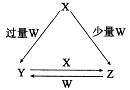
(1)若X为金属单质,W是某强酸的稀溶液。X与少量W反应生成Z的离子方程式为 ,向Y溶液中加入某种试剂 (填试剂名称),若溶液出现血红色,即可判断Y溶液中阳离子的存在。
(2)若X、Y为正盐,X的水溶液显酸性,W为NaOH溶液,写出Y与X在水溶液中转化为Z的离子反应方程式 。
(3)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,溶液的PH变化是 (填“变大”、“变小”、“不变”。不考虑水的挥发),其原因是_________ (用简要的文字说明,并写出离子方程式)。
(4)室温下,若用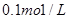 的NaOH溶液滴定
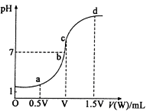
的NaOH溶液滴定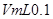 mo1/L HA溶液,滴定曲线如图所示,则a、b、c、d四点溶液中水的电离程度最大的是 点;a点溶液中离子浓度的大小顺序为 ;少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,此时溶液中除H+、OH-外 ,离子浓度的大小顺序为 。
mo1/L HA溶液,滴定曲线如图所示,则a、b、c、d四点溶液中水的电离程度最大的是 点;a点溶液中离子浓度的大小顺序为 ;少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,此时溶液中除H+、OH-外 ,离子浓度的大小顺序为 。

(1)若X为金属单质,W是某强酸的稀溶液。X与少量W反应生成Z的离子方程式为 ,向Y溶液中加入某种试剂 (填试剂名称),若溶液出现血红色,即可判断Y溶液中阳离子的存在。
(2)若X、Y为正盐,X的水溶液显酸性,W为NaOH溶液,写出Y与X在水溶液中转化为Z的离子反应方程式 。
(3)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,溶液的PH变化是 (填“变大”、“变小”、“不变”。不考虑水的挥发),其原因是_________ (用简要的文字说明,并写出离子方程式)。
(4)室温下,若用
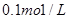 的NaOH溶液滴定
的NaOH溶液滴定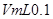 mo1/L HA溶液,滴定曲线如图所示,则a、b、c、d四点溶液中水的电离程度最大的是 点;a点溶液中离子浓度的大小顺序为 ;少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,此时溶液中除H+、OH-外 ,离子浓度的大小顺序为 。
mo1/L HA溶液,滴定曲线如图所示,则a、b、c、d四点溶液中水的电离程度最大的是 点;a点溶液中离子浓度的大小顺序为 ;少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,此时溶液中除H+、OH-外 ,离子浓度的大小顺序为 。
(14分)(1)3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O(2分) 硫氰酸钾或硫氰化钾(1分)
(2)[Al(OH)4]-+3Al3+=4Al(OH)3↓(2分)(或Al3++3AlO2-+6H2O=4Al(OH)3↓)
(3)变小(1分),SO32-有还原性,易被空气中的氧气氧化成SO42-,2SO32-+O2=2SO42-,所以溶液的pH变小(2分,文字1分,离子方程式1分)
(4)c(2分) c(A-)>c(Na+) >c(H+) >c(OH-)(2分);c(Na+) >c(A-) >c(Cl-) (2分)
(2)[Al(OH)4]-+3Al3+=4Al(OH)3↓(2分)(或Al3++3AlO2-+6H2O=4Al(OH)3↓)
(3)变小(1分),SO32-有还原性,易被空气中的氧气氧化成SO42-,2SO32-+O2=2SO42-,所以溶液的pH变小(2分,文字1分,离子方程式1分)
(4)c(2分) c(A-)>c(Na+) >c(H+) >c(OH-)(2分);c(Na+) >c(A-) >c(Cl-) (2分)
试题分析:(1)如果X是金属单质,根据转化可知,X应该是变价金属,所以X应该是Fe。W应该是硝酸,因此X与少量W反应生成Z的离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O。Y溶液中含有铁离子,检验铁离子的试剂是硫氰化钾溶液,即向Y溶液中加入硫氰化钾溶液,若溶液出现血红色,即可判断Y溶液中阳离子的存在。
(2)若X、Y为正盐,X的水溶液显酸性,W为NaOH溶液,这说明X或Y应该是铝的化合物。其中X的水溶液显酸性,X是铝盐,Y是偏铝酸盐,所以Y与X在水溶液中转化为Z的离子反应方程式[Al(OH)4]-+3Al3+=4Al(OH)3↓或Al3++3AlO2-+6H2O=4Al(OH)3↓。
(3)若X为强碱,常温下W为有刺激性气味的气态氧化物,则根据转化关系可知W是SO2。少量SO2与强碱反应生成亚硫酸盐,即Z是亚硫酸盐。由于SO32-有还原性,易被空气中的氧气氧化成SO42-,反应的离子方程式是2SO32-+O2=2SO42-,所以常温时,将Z的水溶液露置于空气中溶液的pH变小。
(4)水是弱电解质,存在电离平衡。酸或碱是抑制水的电离平衡的,盐类水解是促进水的电离平衡。根据图像可知,起始时HA溶液的pH大于1,这说明HA是弱酸。c点酸和碱恰好反应生成NaA,溶液中A-离子水解,所以c点溶液中水的电离程度最大。A点HA过量,溶液显酸性,则溶液中中离子浓度大小顺序是c(A-)>c(Na+) >c(H+) >c(OH-)。少量c点溶液于试管中,再滴加0.1mo1/L盐酸至中性,则根据电荷守恒可知c(Na+) +c(H+)=c(OH-)+c(A-)+c(Cl-),由于c(H+)=c(OH-),所以此时溶液中除H+、OH-外 ,离子浓度的大小顺序是c(Na+) >c(A-) >c(Cl-)。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目

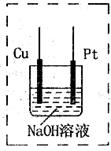
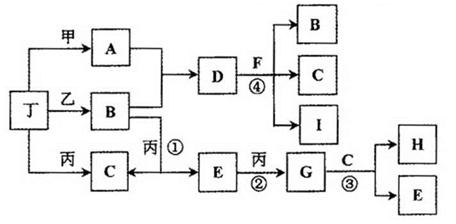
 乙+丁(未配平),达平衡后再加少量B,则平衡 移动(填“正向”、 “逆向”或“不”),重新平衡后与原平衡相比,B的转化率 (填“增大”、 “减小”或“不变”)。
乙+丁(未配平),达平衡后再加少量B,则平衡 移动(填“正向”、 “逆向”或“不”),重新平衡后与原平衡相比,B的转化率 (填“增大”、 “减小”或“不变”)。