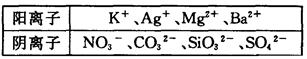题目内容
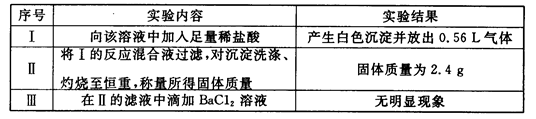
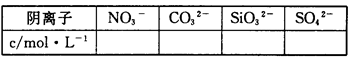
在下列指定条件的溶液中,能大量共存的一组离子是( )
| A.pH=1的溶液中:NH4+、Fe2+、SO42-、ClO- |
| B.通入过量SO2气体后的溶液中:K+、Na+、CO32-、SO42- |
| C.AlO2一 的浓度为0.1 mol/L的溶液中:K+、Na+、SiO32-、SO42- |
| D.常温下,由水电离出的c(H+)=1×10-11 mol/L的溶液中:Fe3+、Br—、Cl-、SCN- |
C
试题分析:A、Fe2+与ClO-不能共存,错误;B、通入过量的SO2后CO32-不能存在,错误;C、正确。 D、Fe3+与SCN-不能共存,错误。

练习册系列答案
相关题目