题目内容
将标准状况下体积为224mL的Cl2通入到25.00mL 0.1mol?L-1 Na2S2O3溶液中恰好完全反应,此时Cl2全部转化为Cl-,则S2O32-转化为( )A.SO42-
B.SO32-
C.S
D.S2-
【答案】分析:反应中Cl2全部转化为Cl-,氯元素化合价由0价降低为-1价,氯元素被还原,Na2S2O3中硫元素被氧化,令硫元素在氧化产物中的化合价为a价,硫元素化合价由+2价升高为a价,表示出得失电子数目,根据电子转移守恒列式方程计算a的值.
解答:解:标准状况下体积为224mL的Cl2的物质的量为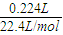 =0.01mol.
=0.01mol.
反应中Cl2全部转化为Cl-,氯元素化合价由0价降低为-1价,氯元素被还原,Na2S2O3中硫元素被氧化,
令硫元素在氧化产物中的化合价为a价,根据电子转移守恒,则:
0.01mol×2=25×10-3L×0.1mol/L×2×(a-2),
解得a=+6,即硫元素被氧化为+6价.
故选A.
点评:本题考查氧化还原反应计算、氧化还原反应概念等,难度中等,表示出得失数目是解题关键.熟练掌握电子转移守恒思想的运用.
解答:解:标准状况下体积为224mL的Cl2的物质的量为
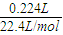 =0.01mol.
=0.01mol.反应中Cl2全部转化为Cl-,氯元素化合价由0价降低为-1价,氯元素被还原,Na2S2O3中硫元素被氧化,
令硫元素在氧化产物中的化合价为a价,根据电子转移守恒,则:
0.01mol×2=25×10-3L×0.1mol/L×2×(a-2),
解得a=+6,即硫元素被氧化为+6价.
故选A.
点评:本题考查氧化还原反应计算、氧化还原反应概念等,难度中等,表示出得失数目是解题关键.熟练掌握电子转移守恒思想的运用.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
将标准状况下体积为2.24L的H2S缓慢通入100ml, 1.5mol/LNaOH溶液中(溶液体积变化忽略不计),充分反应,下列关系错误的是 ( )
| A.c(Na+)+ c(H+)= c(HS-)+2 c(S2-)+ c(OH-) | B.c(Na+)>c(HS-)>c(S2-)>c(H+)>c(OH-) |
| C.c(Na+)>[c(HS-)+c(S2-)+c(H2S)] | D.c(HS-)+c(S2-)+c(H2S)=1.0mol/L |