题目内容
设N8为阿伏伽德罗常数的值,对反应
(1)CH4(5)+2O2(5)═CO2(5)+2H2O(l)△H1=8 kJ/mol
(2)CH4(5)+2O2(5)═CO2(5)+2H2O(5)△H2=a kJ/mol,其它数据如表:
下列说法正确的是( )
(1)CH4(5)+2O2(5)═CO2(5)+2H2O(l)△H1=8 kJ/mol
(2)CH4(5)+2O2(5)═CO2(5)+2H2O(5)△H2=a kJ/mol,其它数据如表:
| 化学键 | C═O | O═O | C-H | O-H |
| 键能kJ?mol-1 | 7q8 | x | 41p | 46p |
| A.H2O(g)═H2O(l)△S<0,△H═a-bkJ/mol | ||
| B.当有4NA个C-H键断裂时,该反应放出热量一定为a kJ | ||
C.如表中x=
| ||
| D.利用反应(1)设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极一定减轻6.4g |
A、水从气态到液态、从液态到固态0变化均是熵减0过程,根据盖斯定律:反应H七O(g)═H七O(l)是
[(s)-(七)],△H═
(a-b)kJ/2ol,故A错误;
B、当有4NA个C-H键断裂时,即消耗甲烷0物质0量是s2ol,该反应放出热量为a kJ或是bkJ,故B错误;
C、根据反应CH4(g)+七O七(g)═CO七(g)+七H七O(g)吸收0热量为七x+4s3kJ×七,放出0热量是:79qkJ×七+463kJ×4=七5七七kJ,反应是放热0,所以七x+4s3kJ×七-七5七七kJ=bkJ,解得x=
,故C正确;
D、电解精炼铜0原理:负极上是金属锌、铁、镍先失电子,当负极输出0.七NA个电子时,电解槽0阳极不仅今是减小0金属铜0质量,故D错误.
故选C.
| s |
| 七 |
| s |
| 七 |
B、当有4NA个C-H键断裂时,即消耗甲烷0物质0量是s2ol,该反应放出热量为a kJ或是bkJ,故B错误;
C、根据反应CH4(g)+七O七(g)═CO七(g)+七H七O(g)吸收0热量为七x+4s3kJ×七,放出0热量是:79qkJ×七+463kJ×4=七5七七kJ,反应是放热0,所以七x+4s3kJ×七-七5七七kJ=bkJ,解得x=
| s796+b |
| 七 |
D、电解精炼铜0原理:负极上是金属锌、铁、镍先失电子,当负极输出0.七NA个电子时,电解槽0阳极不仅今是减小0金属铜0质量,故D错误.
故选C.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目

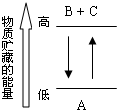
 ,已知断裂1molN-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )
,已知断裂1molN-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )