题目内容
【题目】工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是( )
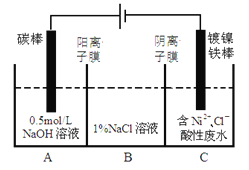
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH— -4e—==O2↑+2H2O
B.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
【答案】B
【解析】
试题分析:A.由图知,碳棒与电源正极相连作电解池的阳极,电极反应为4OH— -4e—=O2↑+2H2O,A正确;B.电解过程中为平衡A、C中的电荷,A中的Na+和C中的Cl-分别通过阳离子膜和阴离子膜移向B中,这使B中NaCl溶液的物质的量浓度不断增大,B错误;C.在弱酸性溶液中易发生水解,且氧化性:Ni2+ (高浓度)>H+>Ni2+(低浓度),为了提高Ni的产率,电解过程中需要控制废水的pH,C正确;D.若将图中阳离子膜去掉,由于放电顺序Cl->OH-,则Cl-移向阳极放电:2Cl-2e-=Cl2↑,电解反应总方程式会发生改变,D正确;答案选B。

练习册系列答案
相关题目