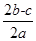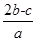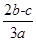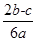题目内容
取pH=4的某电解质溶液 1.00L ,用 Pt电极进行电解,经过一段时间后,测得溶液的pH=1,且阴阳两极产物的物质的量之比为2:1,则该电解质溶液是
| A.盐酸 | B.氯化钾溶液 | C.硝酸银溶液 | D.硫酸铜溶液 |
D
试题分析:根据溶液pH的变化可知,溶液的酸性增强,因此选项B一定是错误的,惰性电极电解氯化钾溶液溶液的碱性增强,且阴阳两极产物的物质的量之比为1:1;惰性电极电极盐酸,阴阳极的电解产物分别是氢气和氯气,物质的量之比是1:1,且溶液的酸性较低,A不正确;惰性电极硝酸银溶液,生成物是银、氧气和硝酸,溶液的酸性增强,但阴阳两极产物的物质的量之比为4:1,C不正确;惰性电极电解硫酸铜溶液生成物是铜、氧气和硫酸,符合题意,答案选D。
点评:该题是中等难度的试题,也是高考中的常见题型和重要的考点。该题综合性强,侧重对学生解题方法的指导与训练,有利于培养学生的应试能力和学习效率。该题的关键是明确电解池中离子的放电顺序,然后结合题意灵活运用即可。

练习册系列答案
相关题目