��Ŀ����
����Ŀ���輰�仯���������������о��й㷺����;��
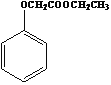
(1)��ҵ�����ֹ�Ļ�ѧ��Ӧ����ʽΪ��SiO2��2C![]() Si���ֹ裩��2CO�����÷�Ӧ�У�����ԭ��Ԫ����___����ԭ����___���ѧʽ������ת��1mol���������ɵ�CO�ڱ�״���µ����Ϊ___L��
Si���ֹ裩��2CO�����÷�Ӧ�У�����ԭ��Ԫ����___����ԭ����___���ѧʽ������ת��1mol���������ɵ�CO�ڱ�״���µ����Ϊ___L��
(2)�ɴֹ��ƴ���Ĺ���Ϊ��
��.�ֹ���������Ӧ�������Ȼ���(SiCl4)��
��.�ڸ�������������ԭ���Ȼ���õ����衣����������Ӧ�Ļ�ѧ����ʽΪ___��
���𰸡�Si C 11.2 2H2+SiCl4![]() Si+4HCl
Si+4HCl
��������
(1)������ѧ����ʽSiO2��2C![]() Si���ֹ裩��2CO����SiԪ�صĻ��ϼ���+4��0�����ϼ۽��ͣ�����ԭ����������������CԪ�صĻ��ϼ���0��+2�����ϼ����ߣ�����������������ԭ�����ɷ�Ӧ����ʽ��֪��ÿ����2molCO����Ӧ��ת��4mol���ӣ���ת��1mol���ӣ�������CO�����ʵ���Ϊ0.5mol���ڱ�״���µ����Ϊ
Si���ֹ裩��2CO����SiԪ�صĻ��ϼ���+4��0�����ϼ۽��ͣ�����ԭ����������������CԪ�صĻ��ϼ���0��+2�����ϼ����ߣ�����������������ԭ�����ɷ�Ӧ����ʽ��֪��ÿ����2molCO����Ӧ��ת��4mol���ӣ���ת��1mol���ӣ�������CO�����ʵ���Ϊ0.5mol���ڱ�״���µ����Ϊ![]() ����Ϊ��Si��C��11.2��
������Si��C��11.2��
(2)��������������ԭ���Ȼ���õ����裬��Ӧ����ʽΪ��2H2+SiCl4![]() Si+4HCl����Ϊ��2H2+SiCl4
Si+4HCl������2H2+SiCl4![]() Si+4HCl��
Si+4HCl��

 ��������ϵ�д�
��������ϵ�д� ����˼ά����ѵ����ʱ��ѧ��ϵ�д�
����˼ά����ѵ����ʱ��ѧ��ϵ�д�����Ŀ��Cu2O�����������������ᣬijѧϰС��̽���Ʊ�Cu2O�ķ�����
���������ϣ��� CuSO4��Na2SO3��Һ��Ͽ��Ʊ�Cu2O���� Cu2OΪש��ɫ���壻��������������Cu2+��Cu��
�� Cu2O��Cu(SO3)23�������ת�� Cu2O![]() Cu(SO3)23-(��ɫ)
Cu(SO3)23-(��ɫ)
(1)����0.25 mol��L��1CuSO4��Һ��0.25 mol��L��1 Na2SO3��Һ�����CuSO4��ҺpH=4��Na2SO3��ҺpH=9�������ӷ���ʽ��ʾCuSO4��ҺpH=4��ԭ��_______��
(2)���CuSO4��Һ��Na2SO3��Һ��Ӧ��Cu2O�����ӷ���ʽ�� ____Cu2++ ____SO32��+ ____ =____Cu2O��+ ____ + ____HSO3��
��ʵ��̽����
���� | ���� |
| i �л�ɫ�������֣����� Na2SO3��Һ�ĵ��룬�������ӣ����ӵ�5 mLʱ����Һ����ɫ��ʧ�� ii ���Թܼ��ȣ���ɫ������Ϊש��ɫ���д̼�����ζ��������� iii�ڼ��������£���������Na2SO3��Һ��ש��ɫ�������٣���1�ӵ�10 mLʱ��������ȫ�ܽ⣬����ɫ��Һ�� |
(3)֤��ii��ש��ɫ������Cu2O��ʵ�鷽����_______��
(4)������i�л�ɫ��������Cu2SO3��ii�г����ɻ�ɫ��ש��ɫ�Ļ�ѧ����ʽ��______��
(5)iii��ש��ɫ������ʧ��ԭ����_______��
(6)�ڼ��������£�����2 mL 0.25 mol��L��1Na2SO3��Һ�еμ�0.25 mol��L��1CuSO4��Һ��������Ԥ�ڹ۲쵽��������_______��
(7)������ʵ��ó����ۣ�CuSO4��Һ��Na2SO3��Һ��Ӧ�Ʊ�Cu2O��Ӧ���Ƶ�������_______��_______��
����Ŀ��(1)��������Ϊ���������ں��º����ܱ������г���һ������NO��NH3����һ�������·�����Ӧ��6NO(g) + 4NH3(g)![]() 5N2(g) +6H2O(g)��
5N2(g) +6H2O(g)��
����˵���÷�Ӧ�Ѵﵽƽ��״̬�ı�־��____________
a����Ӧ���� v( NH3) =v( N2) b��������ѹǿ������ʱ��������仯 c�������� N2 �����ʵ�������������ʱ��������仯 d�������� n(NO)��n(NH3)��n(N2)��n(H2O) = 6��4��5��6 e��12molN-H �����ѵ�ͬʱ���� 5mol N��N �� f��������������������ʱ��ı仯���仯
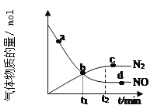
��ij��ʵ���в�������� NO��N2�����ʵ�����ʱ��仯��ͼ��ʾ��ͼ��b���Ӧ�����ʹ�ϵ��v(��) ___________ v(��)�����������d ���Ӧ�����ʹ�ϵ��v(��) ___________ v(��) �����������
(2) ��֪��N��N�ļ���Ϊ946kJ/mol�� H-H�ļ���Ϊ436kJ/mol��N-H�ļ���Ϊ391kJ/mol����N2��H2��Ӧ������1mol NH3������______�����������������ų�����������Ϊ_______kJ��
(3) һ�������£��� 5 L�ܱ������ڣ���Ӧ 2NO2(g) ![]() N2O4(g) ��H��-180 kJ��mol-1��n(NO2)��ʱ��仯���±���
N2O4(g) ��H��-180 kJ��mol-1��n(NO2)��ʱ��仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
���� N2O4 ��ʾ 0��2 s �ڸ÷�Ӧ��ƽ������Ϊ________ molL-1s-1���ڵ� 5s ʱ��NO2 ��ת����Ϊ___________��
�ڸ����ϱ����Կ��������ŷ�Ӧ���У���Ӧ������С����ԭ����______________��
��Ϊ�ӿ췴Ӧ���ʣ����Բ�ȡ�Ĵ�ʩ��_______
a�������¶� b������ʱ����He�� c����ѹʱ����He�� d������ʱ����NO2