题目内容
【题目】为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究。
(1)①把含有较高浓度CO2的空气通入饱和K2CO3溶液。②在①的吸收液中通高温水蒸气得到高浓度的CO2气体。请写出②中反应的化学方程式______。
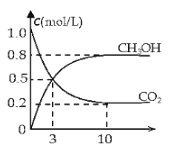
(2)如将CO2与H2以1:3的体积比混合,在适当条件下合成燃料甲醇和水。在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
从反应开始到平衡,v(H2)=______;氢气的转化率=______;能使平衡体系中n(CH3OH)增大的措施有______。(只写一种即可)
【答案】2KHCO3![]() K2CO3+H2O+CO2↑ 0.24mol/(L
K2CO3+H2O+CO2↑ 0.24mol/(L![]() min) 80% 降低温度(或加压或增大H2的量等)
min) 80% 降低温度(或加压或增大H2的量等)
【解析】
(1)①中碳酸钾吸收二氧化碳生成碳酸氢钾,通高温水蒸气,碳酸氢钾分解生成碳酸钾、二氧化碳与水;
(2)由图可知,10min达平衡,平衡时甲醇的浓度变化为0.8mol/L,根据![]() 计算v(CH3OH),再根据速率之比等于化学计量数之比计算v(H2);
计算v(CH3OH),再根据速率之比等于化学计量数之比计算v(H2);
根据CH3OH平衡浓度,利用n=cV计算△n(CH3OH),再根据方程式计算△n(H2),利用转化率等于计算氢气的转化率;
改变体积使平衡向正反应移动,可以增大CH3OH的物质的量,据此结合方程式特征解答。
(1)①中碳酸钾吸收二氧化碳生成碳酸氢钾,通高温水蒸气,碳酸氢钾分解生成碳酸钾、二氧化碳与水,反应方程式为:2KHCO3![]() K2CO3+H2O+CO2↑;
K2CO3+H2O+CO2↑;
故答案为:2KHCO3![]() K2CO3+H2O+CO2↑;
K2CO3+H2O+CO2↑;
(2)由图可知,10min达平衡,平衡时甲醇的浓度变化为0.8mol/L,则10分钟内,v(CH3OH)=0.08mol/(L![]() min),根据速率之比等于化学计量数之比,故v(H2)=3 v(CH3OH)=3×0.08mol/(Lmin)=0.24mol/(L
min),根据速率之比等于化学计量数之比,故v(H2)=3 v(CH3OH)=3×0.08mol/(Lmin)=0.24mol/(L![]() min),平衡时△n(CH3OH)=0.8mol/L×2L=1.6mol,根据方程式可知△n (H2)=3△n(CH3OH)=3×1.6mol=4.8mol,所以氢气的转化率为
min),平衡时△n(CH3OH)=0.8mol/L×2L=1.6mol,根据方程式可知△n (H2)=3△n(CH3OH)=3×1.6mol=4.8mol,所以氢气的转化率为![]() ×100%=80%;
×100%=80%;
该反应正反应是体积减小的放热反应,故降低温度或加压或增大H2的量等,可以是平衡向正反应移动,增大CH3OH的物质的量;
故答案为:0.24mol/(L![]() min);80%;降低温度(或加压或增大H2的量等)。
min);80%;降低温度(或加压或增大H2的量等)。