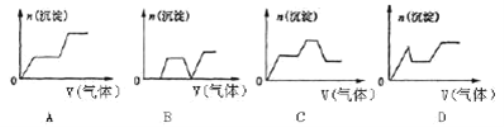
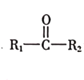��Ŀ����
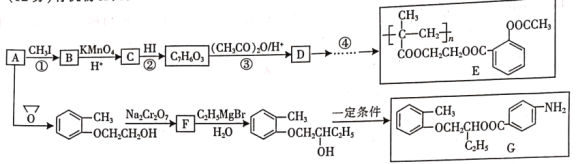
����Ŀ��(1)�л���X��һ����Ҫ���л��ϳ��м��壬�����������ϡ�Ϳ�Ϻ�ճ�ϼ��ȸ߾��Ϊ�о�X�������ṹ������������ʵ�飺
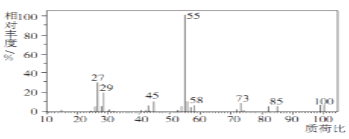
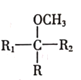
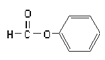
���л���X������ͼΪ��
| �л���X����Է���������________ |
�ڽ�10.0gX������O2�г��ȼ�գ���ʹ���������ͨ����������ˮCaCl2��KOHŨ��Һ��������ˮCaCl2����7.2g��KOHŨ��Һ����22.0g�� | �л���X�ķ���ʽ��__________�� |
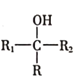
�۾�������ײⶨ���л���X�к���ȩ�����л���X�ĺ˴Ź�������ͼ����2�����շ壬�����֮����3��1�� | �л���X�Ľṹ��ʽ��______ |
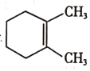
(2)DielsAlder��ӦΪ����˫ϩ�뺬��̼̼˫����̼̼�����Ļ����������������Ԫ��״������ķ�Ӧ����ķ�Ӧ�ǣ�![]() ����A(C5H6)��B��DielsAlder��Ӧ�Ƶá�
����A(C5H6)��B��DielsAlder��Ӧ�Ƶá�
��DielsAlder��Ӧ����________��Ӧ(�Ӧ����)��A�Ľṹ��ʽΪ________��
��д����![]() ��Ϊͬ���칹�壬��һ�����ֻ�����ֵķ����������ƣ�________��д������������һ���������Ҫ�ķ�Ӧ�Լ��ͷ�Ӧ������________��_______
��Ϊͬ���칹�壬��һ�����ֻ�����ֵķ����������ƣ�________��д������������һ���������Ҫ�ķ�Ӧ�Լ��ͷ�Ӧ������________��_______
���𰸡�100 C5H8O2 (CH3)2C(CHO)2 �ӳ�  �����ױ�(��1,3,5���ױ�) �嵥��/���� Һ��/Fe
�����ױ�(��1,3,5���ױ�) �嵥��/���� Һ��/Fe
��������
��������ͼ�ͺ˴Ź�������ȷ���л������Է����������ṹ�����������Ϣ�����л���Ӧ���ͣ�����ȡ����Ӧ��ԭ��������Ӧ��������
(1)������ͼ���ʺɱ������ֵ��Ϊ��Է���������������ͼ��֪�л���X����Է���������100���ʴ�Ϊ��100��
��10.0gX����Ԫ�ص����ʵ���=(7.2g/18g/mol)��2=0.8mol��KOHŨ��Һ����22.0g�Ƕ�����̼������������̼ԭ���غ�֪��̼Ԫ�ص����ʵ���=22.0g/44g/mol=0.5mol��ʣ�ಿ������Ԫ�أ���Ԫ�ص�����Ϊ10.0g0.8��1g0.5��12g=3.2g������Ԫ�ص����ʵ���Ϊ3.2g/16g/mol=0.2mol����÷�����̼���⡢��Ԫ�صĸ���֮��0.5mol:0.8mol:0.2mol=5:8:2�����л���X�ķ���ʽ��C5H8O2��
���л���X�к���ȩ�����л���X�ĺ˴Ź�������ͼ����2�����շ壬������к���2�ֻ�������ԭ�ӣ�����ṹ��ʽΪ(CH3)2C(CHO)2��
(2)��![]() ��A(C5H6)��B��DielsAlder��Ӧ�Ƶã��÷�ӦΪ�ӳɷ�Ӧ����AΪ
��A(C5H6)��B��DielsAlder��Ӧ�Ƶã��÷�ӦΪ�ӳɷ�Ӧ����AΪ![]() ��
��![]() ����
����![]() ���ȶ�����AΪ
���ȶ�����AΪ![]() ��BΪ1��3����ϩ���ʴ�Ϊ���ӳɣ�
��BΪ1��3����ϩ���ʴ�Ϊ���ӳɣ�![]() ��
��
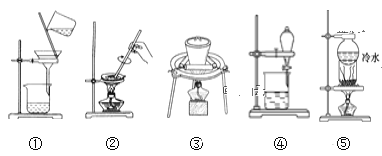
��![]() �ķ���ʽΪC9H12����ͬ���칹���һ�����ֻ�����ֵķ���������3�����ҽṹ�Գƣ�����Ϊ1��3��5�����������������ϵ�ȡ����Ӧ��Ҫ����������Һ�壬�������ϵ�ȡ����Ӧ��Ҫ���պ����������ʴ�Ϊ��1��3��5������������Һ�塢���պ���������
�ķ���ʽΪC9H12����ͬ���칹���һ�����ֻ�����ֵķ���������3�����ҽṹ�Գƣ�����Ϊ1��3��5�����������������ϵ�ȡ����Ӧ��Ҫ����������Һ�壬�������ϵ�ȡ����Ӧ��Ҫ���պ����������ʴ�Ϊ��1��3��5������������Һ�塢���պ���������