题目内容
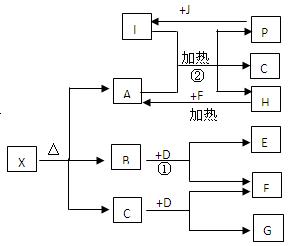
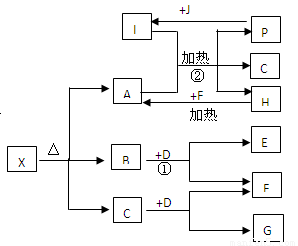
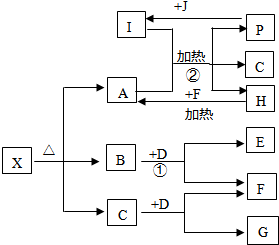
已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有下图所示的关系。
试回答下列问题:
(1)G的化学式为:___________________________________。
(2)写出下列反应的化学方程式
①__________________________________________________________________
②__________________________________________________________________。
(3)X在医药上用作解酸剂,与盐酸作用时,生成B的物质的量与消耗盐酸的物质的量之比为3:8,则X的化学式为:______________________;X与盐酸反应的化学方程式为:_________________________________。
(1)NaOH
(2)①2Na2O2+2CO2====2Na2CO3+O2
②2Mg+CO2![]() 2MgO+C
2MgO+C
(3)3MgCO3·Mg(OH)2或Mg4(OH)2(CO3)3等
3MgCO3·Mg(OH)2+8HCl====4MgCl2+3CO2↑+5H2O
解析:此题考查元素化合物知识,从反应②来看,这是一个金属置换非金属的置换反应,且条件为点燃,考生应联想到2Mg+CO![]() 2MgO+C这个反应,从而可知B为CO2。x为盐,盐分解的产物一般有水,所以x分解后得到MgO、CO2、H2O,从而推出x为碱式碳酸镁。
2MgO+C这个反应,从而可知B为CO2。x为盐,盐分解的产物一般有水,所以x分解后得到MgO、CO2、H2O,从而推出x为碱式碳酸镁。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目

 ①为使数据准确,还需补充装置,请你在方框内绘出装置图并写出试剂名称;
①为使数据准确,还需补充装置,请你在方框内绘出装置图并写出试剂名称;

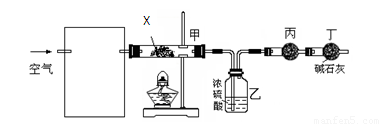
 ①为使数据准确,还需补充装置,请你在方框内绘出装置图并写出试剂名称;
①为使数据准确,还需补充装置,请你在方框内绘出装置图并写出试剂名称;