题目内容
【题目】下列有机物中,既能使溴水褪色,又能使酸性的KMnO4溶液褪色的是( )
A. 乙烯 B. 苯 C. 甲烷 D. 乙酸
【答案】A
【解析】试题分析:既可以使溴水褪色,又可以使酸性KMnO4溶液褪色的有机物应含有碳碳双键或醛基官能团,以此解答该题.
解:A.乙烯含有碳碳双键,可与溴水发生加成反应,与酸性高锰酸钾发生氧化还原反应,故A正确;
B.苯与溴水和酸性高锰酸钾都不反应,故B错误;
C.甲烷与溴水和酸性高锰酸钾都不反应,故C错误;
D.乙酸与溴水和酸性高锰酸钾溶液均不反应,不能使溶液褪色,故D错误.
故选A.

【题目】有关元素X、Y、Z、D、E的信息如下:
元素 | 有关信息 |
X | 元素主要化合价-2,原子半径为0.0074 nm |
Y | 所在主族序数与所在周期序数之差为4 |
Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
请回答下列问题(用化学用语表示):
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为____________。
(2)比较Y与Z的氢化物的稳定性________(用化学式表示)。
(3)E元素与Y元素可形成EY2和EY3两种化合物,则下列说法中正确的是________(填序号)
①通常实验室配制EY3溶液时,可直接用水溶解EY3固体
②EY2不能通过单质直接化合产生
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
④Y、Z、D的离子半径大小依次减小
(4)Y的最高价氧化物为无色液体,当0.25 mol该物质与一定量的水混合得到一种稀溶液时,放出Q kJ的热量,写出该反应的热化学方程式_______________________________。
(5)写出E在潮湿的空气中发生腐蚀时正极上的电极反应式_____________________。
【题目】通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
E(kJ·mol1) | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi-Si键),该反应的产生的热量为( )
Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi-Si键),该反应的产生的热量为( )
A.吸收412 kJ·mol-1 B.放出412 kJ·mol-1
C.吸收236 kJ·mol-1 D.放出236 kJ·mol-1
【题目】(1)用正确的序号填空:
①12C、13C、14C; ②红磷和白磷; ③H2O和D2O;④CH3CH2OH与CH3OCH3; ⑤CH4和CH3CH3 ;
互为同位素的是 ; 互为同素异形体的是 ;
互为同分异构体的是 ; 互为同系物的是
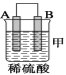
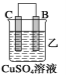
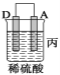
(2)由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 金属A不 断溶解 | C的质 量增加 | A上有气 体产生 |
根据实验现象回答下列问题:
①装置甲中作正极的是_____ ___ (填“A”或“B”)。
②装置乙溶液中Cu2+向_____ __极移动(填“B”或“C”)。
③装置丙中金属A上电极反应属于___ ___(填“氧化反应”或“还原反应”)。
④四种金属活动性由强到弱的顺序是____ ___。