题目内容
【题目】用质量分数为98%,密度为1.84 g·cm-3的浓硫酸配制1 mol/L稀硫酸100 mL,其操作有以下各步:
①用量筒量取一定体积的浓硫酸
②洗涤烧杯和玻璃棒2~3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸转入容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2 cm处,定容,摇匀
完成下列填空:
(1)第①步操作中应用量筒量取__________mL浓硫酸;应选择_________mL量筒(填5、10 或 50)。
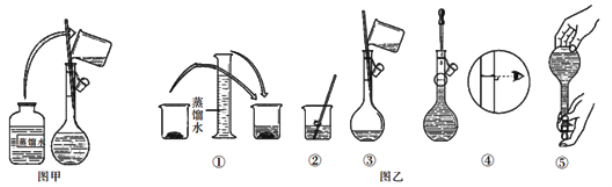
(2)本实验用到的仪器己有烧杯、量筒、玻璃棒,还缺少的仪器是___________。
(3)正确的操作顺序是_________________(用序号填写)。
(4)下列操作会对所配溶液浓度产生什么影响(填“偏高”、“偏低”或“无影响”)
①转移浓硫酸后,小烧杯未洗涤:_______________;
②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中:________________;
③定容时俯视容量瓶刻度线:________________;
④使用前容量瓶未干燥:_________________。
【答案】 5.4 10 100 mL容量瓶、胶头滴管 ①④③②⑤ 偏低 偏高 偏高 无影响
【解析】(1)根据![]() 可知浓硫酸的浓度是
可知浓硫酸的浓度是![]() mol/L=18.4mol/L,因此第①步操作中应用量筒量取浓硫酸的体积为
mol/L=18.4mol/L,因此第①步操作中应用量筒量取浓硫酸的体积为![]() ,所以应选择10mL量筒。(2)本实验用到的仪器己有烧杯、量筒、玻璃棒,还缺少的仪器是100 mL容量瓶、胶头滴管。(3)配制一定物质的量浓度溶液的一般步骤是计算、量取、稀释、冷却、转移、洗涤、摇匀、定容等,所以正确的操作顺序是①④③②⑤。(4)①转移浓硫酸后,小烧杯未洗涤,溶质的物质的量减少,浓度偏低;②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中,溶质的物质的量增加,浓度偏高;③定容时俯视容量瓶刻度线,液面在刻度线下方,体积减少,浓度偏高;④使用前容量瓶未干燥不影响。
,所以应选择10mL量筒。(2)本实验用到的仪器己有烧杯、量筒、玻璃棒,还缺少的仪器是100 mL容量瓶、胶头滴管。(3)配制一定物质的量浓度溶液的一般步骤是计算、量取、稀释、冷却、转移、洗涤、摇匀、定容等,所以正确的操作顺序是①④③②⑤。(4)①转移浓硫酸后,小烧杯未洗涤,溶质的物质的量减少,浓度偏低;②量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中,溶质的物质的量增加,浓度偏高;③定容时俯视容量瓶刻度线,液面在刻度线下方,体积减少,浓度偏高;④使用前容量瓶未干燥不影响。

 快捷英语周周练系列答案
快捷英语周周练系列答案