题目内容
(2012?南开区一模)下列溶液中微粒的物质的量浓度关系正确的是( )
分析:A.碳酸氢钠溶液呈碱性,则溶液中碳酸氢根离子水解程度大于电离程度;
B.根据电荷守恒和物料守恒判断;
C.c(H+)=10-pH;
D.等体积、等物质的量浓度,则NaX和弱酸HX的物质的量相等,利用酸的电离大于盐的水解来分析.
B.根据电荷守恒和物料守恒判断;
C.c(H+)=10-pH;
D.等体积、等物质的量浓度,则NaX和弱酸HX的物质的量相等,利用酸的电离大于盐的水解来分析.
解答:解:A.碳酸氢钠溶液中碳酸氢根离子水解程度大于电离程度,所以c(H2CO3)>c(CO32-),故A错误;
B.根据物料守恒得c(Na+)=2c(S2-)+2c(H2S)+2c(HS-)①,根据电荷守恒得c(Na+)+c(H+)=2c(S2-)+c(OH-)+c(HS-)②,将①带入②得c(OH-)-c(H+)=c(HS-)+2c(H2S),故B错误;
C.pH=3.5的柑橘汁中c(H+)=10-3.5,是pH=6.5的牛奶中c(H+)=10-6.5,所以pH=3.5的柑橘汁中c(H+)是pH=6.5的牛奶中c(H+)的1000倍,故C正确;
D.等体积、等物质的量浓度,则NaX和弱酸HX的物质的量相等,HX的电离大于NaX的水解,则c(X-)>c(Na+),故D错误;
故选C.
B.根据物料守恒得c(Na+)=2c(S2-)+2c(H2S)+2c(HS-)①,根据电荷守恒得c(Na+)+c(H+)=2c(S2-)+c(OH-)+c(HS-)②,将①带入②得c(OH-)-c(H+)=c(HS-)+2c(H2S),故B错误;
C.pH=3.5的柑橘汁中c(H+)=10-3.5,是pH=6.5的牛奶中c(H+)=10-6.5,所以pH=3.5的柑橘汁中c(H+)是pH=6.5的牛奶中c(H+)的1000倍,故C正确;
D.等体积、等物质的量浓度,则NaX和弱酸HX的物质的量相等,HX的电离大于NaX的水解,则c(X-)>c(Na+),故D错误;
故选C.
点评:本题考查离子浓度大小的比较,明确溶液中的电荷守恒式和物料守恒式及弱电解质的电离、盐类的水解是解答本题的关键,易错选项是D,注意电离程度和水解程度的大小,为易错点.

练习册系列答案
相关题目
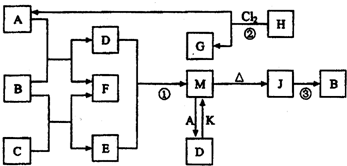 (1)C中存在的化学键类型为
(1)C中存在的化学键类型为