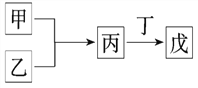
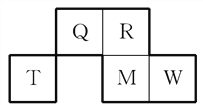
��Ŀ����
����Ŀ������ʵ���о��к���ɫ����������Աȷ������ý��۲���ȷ���ǣ� ��
|
|
|
�� | �� | �� |
A. �ɢ��еĺ���ɫ���壬�ƶϲ���������һ���ǻ������
B. ����ɫ���岻�ܱ�������ľ̿��Ũ���ᷢ���˷�Ӧ
C. �ɢ��Ʋ�Ũ������лӷ��ԣ������ĺ���ɫ����Ϊ��ԭ����
D. �۵���������м�CO2���ɴ�˵��ľ̿һ����Ũ���ᷢ���˷�Ӧ
���𰸡�D
��������A�������к���ɫ���壬˵��������NO2������������ԭ��Ӧ���ɣ���Ӧǰ��Ԫ�صĻ��ϼ۽��ͣ�˵����Ȼ��Ԫ�ػ��ϼ����ߣ�����Ԫ��ֻ������Ԫ�أ���˱�Ȼ���������ɡ����Կ��ƶϲ���������һ���ǻ�����壬ѡ��A��ȷ��B�����������ֽܷ����NO2�����Ԣ��в����ĺ���ɫ���岻һ����ľ̿��Ũ���ᷴӦ�����ģ����п���������ֽ�����ģ�ѡ��B��ȷ��C�����к���ɫ�������Դһ�������ᣬ�����Ტû�������ľֱ̿�ӽӴ�����Ȼ������ӷ������ı仯������������Ļӷ��ԡ�����NO2����������ֽ�����ģ����������ľ̿��Ӧ�����ģ���Ϊ�����е�Ԫ�ؽ��ۺ�IJ������ԭ�����ѡ��C��ȷ��D���۵���������м���CO2���п�����ľ̿���ӷ�����Ũ�������������ģ�����Ϊ�Թ��DZ�¶�ڿ����еģ�Ҳ�п����Ǻ��ȵ�ľ̿�������е�������������ֽ�����������������ģ�ѡ��D����ȷ����ѡD��
�㾦������ͻ�������˻���ʵ����ʵ�ͻ���֪ʶ���ܵĿ�ѧ���������������ʵ����ʵ�ص��ע�����Ƕȣ�1.ʵ��������ɫ���壻2.ʵ�����������ȣ�3. ʵ�黷��������������
�����͡���ѡ��
��������
15
����Ŀ������֪34Se��ԭ�ӽṹʾ��ͼ��ͼ��ʾ���ش��������⣺

��1��Se��Ԫ�����ڱ��е�λ����__________��
��2����Se�����ڱ��е�λ�÷����ж�����˵����ȷ����__________��
A�����ȶ��ԣ�PH3>H2S>H2Se B����ԭ�ԣ�H2Se>HBr>HCl
C�����Ӱ뾶��Se2->Cl->K+ D�����ԣ�HClO3>HBrO3>H2SeO3
�����¶�t1��t2�£�X2(g)��H2��Ӧ����HX��ƽ�ⳣ�����±���
��ѧ����ʽ | K(t1) | K(t2) |
F2+H2===2HF | 1.8��1036 | 1.9��1032 |
Cl2+H2===2HCl | 9.7��1012 | 4.2��1011 |
Br2+H2===2HBr | 5.6��107 | 9.3��106 |
I2+H2===2HI | 43 | 34 |
��1����֪��HX�����ɷ�Ӧ�Ƿ��ȷ�Ӧ�����¶�t2__________t1���<����>������
��2���õ���ʽ��ʾHX���γɹ���__________��
��3�����ۼ��ļ����湲�õ��Ӷ�ƫ�Ƴ̶ȵ��������ǿ��HX���ۼ��ļ�����ǿ������˳����__________��
��4��X2������H2��Ӧ����HX����ԭ�ӽṹ����ԭ��__________��
��5��K�ı仯���ֳ�X2��ѧ���ʵĵݱ��ԣ���ԭ�ӽṹ����ԭ��__________��ԭ�Ӱ뾶�����õ�������������
��6��������K�ı仯�������ƶϳ�������±��ԭ�Ӻ˵���������ӣ�__________��ѡ����ĸ����
a������ͬ�����£�ƽ��ʱX2��ת�������� b��HX���ȶ�������
c��X2��H2��Ӧ�ľ��ҳ̶����� d��HX�Ļ�ԭ������
��7����ͬ±��ԭ��֮����γ�±�ػ������������±�ص��������д��BrCl��SO2��ˮ��Һ�з�����Ӧ�Ļ�ѧ����ʽ__________��
���𰸡� ��4���ڵڢ�A�� BC > ![]() HF��HCl��HBr��HI ±��ԭ�ӵ���������������7 ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ����������� ab BrCl+SO2+2H2O=H2SO4+HCl+HBr
HF��HCl��HBr��HI ±��ԭ�ӵ���������������7 ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ����������� ab BrCl+SO2+2H2O=H2SO4+HCl+HBr
��������I.(1). ����Se��ԭ�ӽṹʾ��ͼ��֪��Se���ĸ����Ӳ㣬�������6�����ӣ�����Ӳ�������������������������������������������SeԪ��λ��Ԫ�����ڱ��ĵ�4���ڵ�VIA�壬�ʴ�Ϊ����4���ڵ�VIA����
(2). A. ͬһ���ڴ�����Ԫ�صķǽ���������ǿ��ͬһ������ϵ���Ԫ�صķǽ�������������ǽ�����S��P��S��Se������Ԫ�صķǽ�����Խǿ������̬�⻯�����ȶ���Խǿ���������ȶ���H2S��PH3��H2S��H2Se����A����B. �ǽ�����Cl��Br��Se����ǽ�����Խǿ�����Ӧ�����ӵĻ�ԭ��Խ������ԭ�ԣ�H2Se>HBr>HCl����B��ȷ��C. ���Ӳ���Խ�࣬���Ӱ뾶Խ�������Ӱ뾶Se2->Cl-��������ͬ��������Ų������ӣ�ԭ������Խ�����Ӱ뾶ԽС�������Ӱ뾶Cl->K+���������Ӱ뾶��Se2->Cl->K+����C��ȷ��D. ����������Ӧ��ˮ��������Խǿ��Ԫ�صķǽ�����Խǿ����HClO3��HBrO3��H2SeO3�����Ǹ�Ԫ�ص�����������Ӧ��ˮ����������Ƚ�����ǿ������D����ѡBC��
II. (1). ��HX�����ɷ�Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С���ɱ������ݿ�֪��K(t1)��K(t2)��˵��t2��t1���ʴ�Ϊ������
(2). ��HX���ǹ��ۻ������ԭ������������Xԭ�����������γ�һ�Թ��õ��Ӷԣ����γɹ��̿ɱ�ʾΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(3). F��Cl��Br��I���ڢ�A��Ԫ�أ�ͬ����Ԫ�����϶������ź˵����������ԭ�Ӻ�����Ӳ��������࣬����ԭ�Ӱ뾶���������ԭ�Ӻ˶��������ӵ��������������Ӷ����·ǽ�������������������Ԫ�صõ����ӵ���������������HF���ļ�����ǿ��HI�ļ������������HX���ۼ��ļ�����ǿ������˳����HF��HCl��HBr��HI���ʴ�Ϊ��HF��HCl��HBr��HI��
(4). ±��ԭ�ӵ�������������Ϊ7�����ڷ�Ӧ�о��õ�1�����Ӷ��ﵽ8���ӵ��ȶ��ṹ����Hԭ���������һ�����ӣ��ڷ�Ӧ��Ҳ�ܵõ�1�����Ӷ��ﵽ2���ӵ��ȶ��ṹ�����±�ص�������������ʱ��ͨ��һ�Թ��õ��Ӷ��γɻ�����HX���ʴ�Ϊ��±��ԭ�ӵ���������������7��
(5). ƽ�ⳣ��Խ��˵����ӦԽ���У�F. Cl��Br��I�ĵõ����������μ�С����Ҫԭ���ǣ�ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ����������࣬ԭ�Ӱ뾶�����õ�������������ɵģ��ʴ�Ϊ��ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ�������������
(6). a. KֵԽ��˵����Ӧ������̶�Խ��ת����Խ�ߣ���a��ȷ��b. ��Ӧ������̶�ԽС��˵��������Խ���ȶ�����b��ȷ����ѡ��c��d����K�Ĵ�С��ֱ�ӹ�ϵ����c��d����ѡab��
(7). ��ͬ±��ԭ��֮����γ�±�ػ������������±�ص�������������������������Ӧ����HCl�������ԭ�������ƶ�BrCl��SO2��ˮ��Һ�з�����Ӧ�Ļ�ѧ����ʽΪ��BrCl+SO2+2H2O=H2SO4+HCl+HBr���ʴ�Ϊ��BrCl+SO2+2H2O=H2SO4+HCl+HBr��

 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�����Ŀ������ͭ��һ��Ӧ�ü���㷺�Ļ���ԭ�ϣ�������ij�����ú�����ͭΪԭ������������CuSO4��5H2 O��������ʯ�ࣨCaSO4��2H2O������������ʾ��ͼ��

������ʯ���ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ�����±���
�¶�( | 20 | 40 | 60 | 80 | 100 |
ʯ�ࣨg�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
������g�� | 32 | 44.6 | 61.8 | 83.8 | 114 |
��ش��������⣺
��1������ɫ��������Ҫ�ɷ���__________________��
��2��д����������������ͭ���ӵ����ӷ���ʽ________________________________________��
��3������I��������Ũ����__________�Ȳ������¶�Ӧ�ÿ�����_____![]() ���ң�
���ң�
��4������Һ�з��������ͭ���������Ӧ����_______�ᾧ����������ˮ�Ҵ���ϴ��Һ����������ˮ��ԭ����_______________________________________������ʱ�������ɣ����ü��Ⱥ�ɵ�ԭ����_________________________��