��Ŀ����
8�����л�ѧ��Ӧ�����ӷ���ʽ����H++OH-�TH2O��ʾ���ǣ�������| A�� | H2SO4+Ba��OH��2�TBaSO4+2H2O | B�� | 2NaOH+H2SO4�T2H2O+Na2SO4 | ||
| C�� | CH3COOH+NaOH�TCH3COONa+H2O | D�� | HNO3+KOH�TKNO3+H2O |
���� H++OH-�TH2O��ʾ������ǿ����߿�����ǿ�����ʽ����ǿ�Ӧ���ɿ������κ�ˮ���ݴ˽��
��� �⣺A��H2SO4+Ba��OH��2�TBaSO4+2H2O�����ӷ���ʽ��Ba2++2OH-+2H++SO42-�TBaSO4��+2H2O����A��ѡ��
B.2NaOH+H2SO4�T2H2O+Na2SO4����Ӧʵ��Ϊ�����������������ӷ�Ӧ����ˮ�����ӷ���ʽ��H++OH-�TH2O����Bѡ��
C������Ϊ���ᣬӦ������ѧʽ�����ӷ���ʽ��CH3COOH+OH-�TCH3COO-+H2O����C��ѡ��
D��HNO3+KOH�TKNO3+H2O����Ӧʵ��Ϊ�����������������ӷ�Ӧ����ˮ�����ӷ���ʽ��H++OH-�TH2O����Dѡ��
��ѡ��BD��
���� ���⿼�������ӷ���ʽ���������д����ȷ���ӷ���ʽ��д�����ͷ�Ӧʵ���ǽ���ؼ�����Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
18��һ������CuS��Cu2S�Ļ����Ͷ��������ŨHNO3�У��ռ���NO2����VL����״��������Ӧ�����Һ�У�����Cu2+��SO42-����������NaOH��������ɫ���������ˣ�ϴ�ӣ����գ��õ�CuOΪ8.0g����V����Ϊ��������
| A�� | 9.0L | B�� | 11.2L | C�� | 16.8L | D�� | 17.92L |
19������˵����ȷ���ǣ�������
| A�� | ζ��������ζ��ʳ�T����ʳ�� | |
| B�� | ��ʯ�ҿɷ�ֹʳ���ܳ������ۿɷ�ֹʳ���������� | |
| C�� | ��֬�����ۡ������ʺ�ά���صȾ�Ϊ�߷��ӻ����� | |
| D�� | ʳƷ���Ӽ������������ж�������Ӧ�ý�ֹ����ʳƷ���Ӽ� |
16����NA��ʾ�����ӵ�������������������ȷ���ǣ�������
| A�� | ���³�ѹ�£�11.2L NH3������ԭ����Ϊ2NA | |
| B�� | ���³�ѹ�£�80g SO3���е���ԭ����Ϊ3NA | |
| C�� | ��״���£�22.4L H2������ԭ����ΪNA | |
| D�� | 56gCO�����ķ�����Ϊ3NA |
3�����л�ѧʵ�����ע�ⰲȫ������˵������ȷ���ǣ�������
| A�� | �������ὦ�����У�Ӧ������ˮ��ϴ����ϴ��գ�۾� | |
| B�� | ������Ũ��մ��Ƥ���ϣ�Ӧ�����ô���ˮ��ϴ��Ȼ��Ϳ��������Һ | |
| C�� | ʵ�����н��п�ȼ������ȼ������ʵ��ʱ���������鴿�����ȼ | |
| D�� | ����ϡ����ʱ����������Ͳ�м�һ�������ˮ�����ڽ�������������Ũ���� |
13���������ֱ����뷴Ӧ����ʽ��Ӧ����ȷ���ǣ�������
| A�� | ʵ������Һ��ͱ��ڴ������������屽��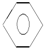 +Br2$\stackrel{FeBr_{3}}{��}$ +Br2$\stackrel{FeBr_{3}}{��}$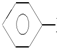 Br+HBr Br+HBr | |
| B�� | ������Һ��ͨ������CO2��2C6H5O-+CO2+H2O��2C6H5OH+CO32- | |
| C�� | 1 L0.5 mol/Lϡ������1 L1 mol/L����������Һ��Ӧ�ų�57.3 kJ���ȣ�H2SO4��aq��+2NaOH��aq���TNa2SO4��aq��+2H2O��l������H=-57.3 kJ/mol | |
| D�� | ��ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��H2��g��+$\frac{1}{2}$O2��g��=H2O��g������H=-241.8kJ/mol |
20���������ʵ���״���෨�ͽ�����෨������H2SO4�ķ�����ȷ���ǣ�������
��� ������� ���⻯� ��ǿ� �ݺ�������ѻӷ���� ��һԪ� ���� �����
��� ������� ���⻯� ��ǿ� �ݺ�������ѻӷ���� ��һԪ� ���� �����
| A�� | �٢ܢݢޢ� | B�� | �٢ڢܢݢޢߢ� | C�� | �٢ۢܢݢޢ� | D�� | �٢ܢݢޢߢ� |
17������˵���в���ȷ���ǣ�������
| A�� | 1mol笠������к��еĵ�����Ϊ9NA | |
| B�� | 16g�����ͳ����Ļ�����к���NA����ԭ�� | |
| C�� | 8g����������������õ��Ӷ���Ϊ2NA | |
| D�� | 31g����P4�к���0.25NA���������幹�͵ķ��� |
18����ͼ��ʾװ�ã��ܹ����ԭ����������ݲ������ǣ�������
| A�� | 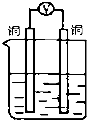 ϡ���� | B�� | 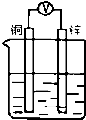 ϡ���� | C�� | 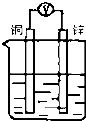 ����ͭ��Һ | D�� |  �Ҵ���Һ |