题目内容
18.在一定条件下,在密闭容器中进行的反应aX(g)+bY(g)?cZ(g)+dW(g),5min后达到平衡,X减少n mol•L-1,Y减少n/3mol•L-1,Z增加2n/3mol•L-1.在其他条件不变时,将容器体积增大,W的百分含量不发生变化.则化学方程式中各物质的化学计量数之比a:b:c:d应为( )
| A. | 1:3:1:2 | B. | 3:1:2:2 | C. | 3:1:2:1 | D. | 1:3:2:2 |
分析 根据反应中各物质的浓度变化量之比等于化学计量数之比确定a、b、c的比值,根据增大压强平衡不移动,则反应前后气体的计量数相等,可确定化学方程式的计量数d与a、b、c的关系,据此答题.
解答 解:反应中各物质的浓度变化量之比等于化学计量数之比,则a:b:c=n:$\frac{n}{3}$:$\frac{2n}{3}$=3:1:2,增大压强W的百分含量不发生变化,即平衡不移动,则反应前后气体的计量数相等,可得a+b=c+d,即3+1=2+d,则d=2,所以a:b:c:d=3:1:2:2,故选B.
点评 本题主要考查了化学反应速率有关计算、压强对化学平衡的影响,难度不大,原理基础知识的理解巩固.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
9.下列有关钠元素等的叙述中,错误的是( )
| A. | 单质钠熔点低于100℃ | |
| B. | 钠元素只能以化合态存在于自然界 | |
| C. | Na与Na+都具有强的还原性 | |
| D. | 金属钠具有好的导电性,但日常中不用作导线 |
6.下列元素中,族序数等于元素在周期表中的周期数的整数倍的是( )
| A. | O | B. | F | C. | P | D. | Cl |
13.在隔绝空气的情况下,9.2g铁、镁、铝混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到4.48L(标准状况下)NO气体.在反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为( )
| A. | 18.6 g | B. | 20 g | C. | 19.4 g | D. | 24 g |
3.线型弹性材料“丁苯吡橡胶”的结构简式如下:
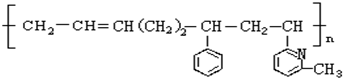
其单体可能是以下6种中的正确的组合是( )
①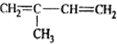 ②
②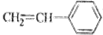 ③CH2=CH-CH=CH2④
③CH2=CH-CH=CH2④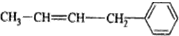 ⑤
⑤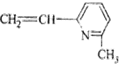 ⑥
⑥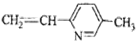
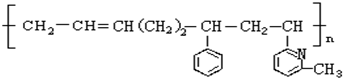
其单体可能是以下6种中的正确的组合是( )
①
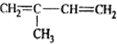 ②
②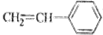 ③CH2=CH-CH=CH2④
③CH2=CH-CH=CH2④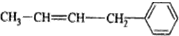 ⑤
⑤ ⑥
⑥
| A. | ②③⑤ | B. | ②③⑥ | C. | ①②⑥ | D. | ②④⑥ |
10.下列化学式只表示一种纯净物的是( )
| A. | C3H8 | B. | C4H10 | C. | C3H6 | D. | C |
7.下列离子方程式中正确的是( )
| A. | 将少量SO2气体通入氨水中:SO2+NH3•H2O═NH4++HSO3- | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| C. | 向NaOH溶液中滴入少量AlCl3溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 向稀硫酸加入少量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
8.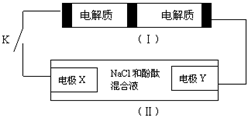 下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:
下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:
2Na2S2+NaBr3化气 $?_{充电}^{放电}$ Na2S4+3NaBr
当闭合开关K时,X电极附近溶液变红.下列说法正确的是( )
 下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:
下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:2Na2S2+NaBr3化气 $?_{充电}^{放电}$ Na2S4+3NaBr
当闭合开关K时,X电极附近溶液变红.下列说法正确的是( )
| A. | 闭合开关K时,钠离子从右到左通过离子交换膜 | |
| B. | 闭合开关K时,负极反应式为:3NaBr-2e-═NaBr3+2Na+ | |
| C. | 闭合开关K时,X电极反应式为:2Cl--2e-═Cl2↑ | |
| D. | 闭合开关K时,当有0.1molNa+通过离子交换膜,X电极上析出标准状况下气体1.12L |