题目内容
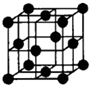
(6分)相对原子质量均大于10的A、B两种元素可化合成X、Y两种气体化合物,1分子X中含A、B原子各1个,1分子Y中含1个A原子和m个B原子。已知7.0 g X在标准状况下的体积约为5.6 L,同温同压下1.0 L Y(g)的质量与22 L氢气的质量相等。通过计算分析A、B各是何种元素?X、Y各是何种化合物?
【答案】
A为碳元素,B为氧元素;X为CO,Y为CO2。
【解析】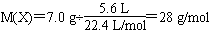
由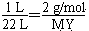 可得,M(Y)=44 g/mol
可得,M(Y)=44 g/mol
X的化学式为AB,设Y的化学式为ABm,并设A、B的相对原子质量分别为a、b(a>10,b>10)[则 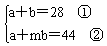
由①②得(m-1)b=16
因m为正整数,又b>10,所以m只能等于2,则b=16,对应B为氧元素,a=12,对应A为碳元素。

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目