ΧβΡΩΡΎ»ί
Μ·―ß”κ…ζΜνΓΔ…γΜαΖΔ’ΙœΔœΔœύΙΊΘ§œ¬Ν–”–ΙΊΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A. ΓΑ ±Τχ¥μΡφΘ§ω≤Έμ±Έ»’Γ±Θ§ΈμΥυ–Έ≥…ΒΡΤχ»ήΫΚΡή≤ζ…ζΕΓ¥οΕϊ–ß”Π
B. ΓΑ«ύίο“ΜΫ“Θ§“‘Υ°Εΰ…ΐάΘΘ§Ϋ »Γ÷≠Γ±Θ§ΆάΏœΏœΧα»Γ«ύίοΥΊΒΡΙΐ≥Χ÷–ΖΔ…ζΝΥΜ·―ß±δΜ·
C. ΓΑΑΨΒ®Ζ·ΧζΗΣΘ§ΨΟ÷°“ύΜ·ΈΣΆ≠Γ±Θ§±±ΥΈ…ρά®”ΟΒ®Ζ·ΝΕΆ≠ΒΡΙΐ≥Χ τ”Ύ÷ΟΜΜΖ¥”Π
D. ΓΑΆβΙέ»γ―©Θ§«Ω…’÷°Θ§Ήœ«ύ―ΧΤπΓ±Θ§Ρœ±±≥·Χ’ΚκΨΑΕ‘œθΥαΦΊΒΡΦχΕ®Ιΐ≥Χ÷–άϊ”ΟΝΥ―φ…ΪΖ¥”Π
 –«ΦΕΩΎΥψΧλΧλΝΖœΒΝ–¥πΑΗ
–«ΦΕΩΎΥψΧλΧλΝΖœΒΝ–¥πΑΗ¥”Μ·―ßΦϋΒΡΫ«Ε»Ζ÷ΈωΘ§Μ·―ßΖ¥”ΠΒΡΙΐ≥ΧΨΆ «Ζ¥”ΠΈοΒΡΜ·―ßΦϋΒΡΕœΝ―ΚΆ…ζ≥…ΈοΒΡΜ·―ßΦϋΒΡ–Έ≥…Ιΐ≥ΧΓΘ
“―÷ΣΦϋΡή ΐΨί»γœ¬±μΘΚ
Μ·―ßΦϋ | NΓ‘N | NΓΣH | HΓΣH |
ΦϋΡή(kJ/mol) | 942 | 391 | b |
Ζ¥”ΠN2(g)+3H2(g)  2NH3(g)ΘΜΓςH=-93kJΓΛmol-1ΓΘ ‘ΗυΨί±μ÷–ΥυΝ–ΦϋΡή ΐΨίΦΤΥψb ΐ÷ΒΘΚ
2NH3(g)ΘΜΓςH=-93kJΓΛmol-1ΓΘ ‘ΗυΨί±μ÷–ΥυΝ–ΦϋΡή ΐΨίΦΤΥψb ΐ÷ΒΘΚ
A. 551 B. 437 C. 558 D. 160
“‘Ρ≥Κ§Ά≠Ωσ ·[÷ς“Σ≥…Ζ÷ΈΣFeCu4SiO5Θ®OHΘ©4Θ§Κ§…ΌΝΩSiO2ΓΔCuCO3]ΈΣ‘≠ΝœΘ§÷Τ±ΗCuSO4ΓΛ5H2OΒΡΝς≥Χ»γœ¬ΘΚ
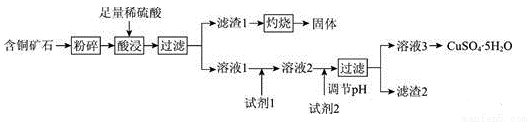
“―÷ΣΘΚ
ΔΓΘ°»ή“Κ÷–άκΉ”≈®Ε»–Γ”ΎΒ»”Ύ1.0ΓΝ10Θ≠5molΓΛLΘ≠1 ±Θ§»œΈΣΗΟάκΉ”≥ΝΒμΆξ»ΪΓΘ
ΔΔΘ°œύΙΊ ‘ΦΝ≥…Ζ÷ΚΆΦέΗώ»γ±μ1Υυ ΨΓΘ
ΔΘΘ°25Γφ ±Θ§ΗΟΝς≥Χ÷–Ϋπ τάκΉ”…ζ≥…«β―θΜ·Έο ±Θ§ΩΣ Φ≥ΝΒμΚΆ≥ΝΒμΆξ»ΪΒΡpH»γ±μ2Υυ ΨΓΘ
±μ1
‘ΦΝ | ≥…Ζ÷ | ΦέΗώΘ·Θ®‘ΣΓΛΕ÷Θ≠1Θ© |
Τ·ΑΉ“Κ | Κ§25.2ΘΞNaClO | 450 |
ΥΪ―θΥ° | Κ§30ΘΞH2O2 | 2400 |
≈®œθΥα | Κ§98ΘΞHNO3 | 1500 |
±μ2
«β―θΜ·Έο | ΩΣ Φ≥ΝΒμΒΡpH | ≥ΝΒμΆξ»ΪΒΡpH |
FeΘ®OHΘ©2 | 7.6 | 9.6 |
FeΘ®OHΘ©3 | 2.7 | 3.7 |
CuΘ®OHΘ©2 | 4.0 | 6.5 |
«κΜΊ¥πΘΚ
Θ®1Θ©FeCu4SiO5Θ®OHΘ©4”Ο―θΜ·ΈοΒΡ–Έ ΫΩ…±μ ΨΈΣ________ΓΘ
Θ®2Θ©ΫαΚœΧβ÷––≈œΔΘ§Υυ―Γ”ΟΒΡ ‘ΦΝ1ΒΡΟϊ≥ΤΈΣ________ΘΜΦ”»κΗΟ ‘ΦΝ ±Θ§ΥυΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ________ΓΘ
Θ®3Θ©Φ”»κ ‘ΦΝ2Θ§–ηΒςΫΎ»ή“ΚΒΡpHΒΡΚœάμΖΕΈßΈΣ________ΓΘ ‘ΦΝ2Ω…“‘―Γ‘ώœ¬Ν–Έο÷ ÷–ΒΡ________Θ®ΧνΉ÷ΡΗΘ©ΓΘ
AΘ°Cu BΘ°CuO
CΘ°CuΘ®OHΘ©2 DΘ°Fe
Θ®4Θ©25Γφ ±Θ§CuΘ®OHΘ©2ΒΡ»ήΕ»Μΐ≥Θ ΐKsp[CuΘ®OHΘ©2]ΘΫ________ΓΘ
Θ®5Θ©CuSO4ΓΛ5H2O»ή“ΚΩ…”Ο”ΎΒγΫβΨΪΝΕΆ≠ΓΘΒγΫβΨΪΝΕΆ≠ ±Θ§ΒΦœΏ÷–Ά®Ιΐ9.632ΓΝ104CΒΡΒγΝΩ ±Θ§άμ¬έ…œ“θΦΪ÷ ΝΩ‘ωΦ”________gΓΘΘ®“―÷ΣΘΚ1ΗωΒγΉ”ΒΡΒγΝΩΈΣ1.6ΓΝ10Θ≠19CΘ©
Μ·―ß‘Ύ…ζ≤ζΓΔ…ζΜν÷–”–ΙψΖΚ”Π”ΟΘ§œ¬Ν–Ε‘”ΠΙΊœΒ’ΐ»ΖΒΡ «
―Γœν | Μ·―ß–‘÷ | ΒΦ ”Π”Ο |
A | ΧΦ‘ΣΥΊΒΡΖ«Ϋπ τ–‘±»Ιη«Ω | ·”ΔΚΆΧΦΖέΒΡΜλΚœΈοΗΏΈ¬œ¬Ζ¥”Π÷Τ±Η¥÷Ιη |
B | ““¥ΦΡή ΙΒΑΑΉ÷ ±δ–‘ | ΈόΥ°““¥ΦΉς“Ϋ”ΟœϊΕΨΦΝ |
C | ΟςΖ·»ή“Κœ‘Υα–‘ | ΟςΖ·ΉςΨΜΥ°ΦΝ |
D | ”Ά÷§‘ΎΦν–‘ΧθΦΰœ¬Υ°Ϋβ | »»ΒΡNaOH»ή“ΚΦχ±π÷≤Έο”ΆΚΆΩσΈο”Ά |
A. A B. B C. C D. D
¥ΦΆ―Υ° «Κœ≥…œ©ΧΰΒΡ≥Θ”ΟΖΫΖ®Θ§ Β―ι “Κœ≥…ΜΖΦΚœ©ΒΡΖ¥”ΠΚΆ Β―ιΉΑ÷Ο»γœ¬ΘΚ
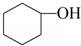

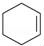 +H2O
+H2O
Ω…Ρή”ΟΒΫΒΡ”–ΙΊ ΐΨί»γœ¬ΘΚ
œύΕ‘Ζ÷Ή”÷ ΝΩ | ΟήΕ»/Θ®g•cm©¹3Θ© | Ζ–Βψ/Γφ | »ήΫβ–‘ | |
ΜΖΦΚ¥Φ | 100 | 0.961 8 | 161 | ΈΔ»ή”ΎΥ° |
ΜΖΦΚœ© | 82 | 0.810 2 | 83 | Ρ―»ή”ΎΥ° |
Κœ≥…Ζ¥”ΠΘΚ
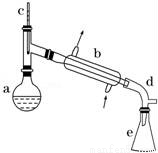
‘Ύa÷–Φ”»κ20gΜΖΦΚ¥ΦΚΆ2–ΓΤ§Υι¥…Τ§Θ§ά以ΫΝΕ·œ¬¬ΐ¬ΐΦ”»κ1mL≈®ΝρΥαΘ°b÷–Ά®»κά以հΚσΘ§ΩΣ ΦΜΚ¬ΐΦ”»»aΘ§ΩΊ÷ΤΝσ≥ωΈοΒΡΈ¬Ε»≤Μ≥§Ιΐ90ΓφΘ°
Ζ÷άκΧα¥ΩΘΚ
Ζ¥”Π¥÷≤ζΈοΒΙ»κΖ÷“Κ¬©ΕΖ÷–Ζ÷±π”Ο…ΌΝΩ5%ΧΦΥαΡΤ»ή“ΚΚΆΥ°œ¥Β”Θ§Ζ÷άκΚσΦ”»κΈόΥ°¬»Μ·ΗΤΩ≈ΝΘΘ§Ψ≤÷Ο“ΜΕΈ ±ΦδΚσΤζ»Ξ¬»Μ·ΗΤΘ°Ήν÷’Ά®Ιΐ’τΝσΒΟΒΫ¥ΩΨΜΜΖΦΚœ©10gΘ°
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©ΉΑ÷ΟbΒΡΟϊ≥Τ «__________Θ°
Θ®2Θ©Φ”»κΥι¥…Τ§ΒΡΉς”Ο «_________ΘΜ»γΙϊΦ”»»“ΜΕΈ ±ΦδΚσΖΔœ÷ΆϋΦ«Φ”¥…Τ§Θ§”ΠΗΟ≤…»ΓΒΡ’ΐ»Ζ≤ΌΉς «________Θ®Χν’ΐ»Ζ¥πΑΗ±ξΚ≈Θ©Θ°
AΘ°ΝΔΦ¥≤ΙΦ” BΘ°ά以Κσ≤ΙΦ” CΘ°≤Μ–η≤ΙΦ” DΘ°÷Ί–¬≈δΝœ
Θ®3Θ©±Ψ Β―ι÷–Ήν»ί“Ή≤ζ…ζΒΡΗ±≤ζΈοΒΡΫαΙΙΦρ ΫΈΣ________________________Θ°
Θ®4Θ©Ζ÷“Κ¬©ΕΖ‘Ύ Ι”Ο«Α–κ«εœ¥Η…ΨΜ≤Δ__________ΘΜ‘Ύ±Ψ Β―ιΖ÷άκΙΐ≥Χ÷–Θ§≤ζΈο”ΠΗΟ¥”Ζ÷“Κ¬©ΕΖΒΡ______________Θ®ΧνΓΑ…œΩΎΒΙ≥ωΓ±ΜρΓΑœ¬ΩΎΖ≈≥ωΓ±Θ©Θ°
Θ®5Θ©Ζ÷άκΧα¥ΩΙΐ≥Χ÷–Φ”»κΈόΥ°¬»Μ·ΗΤΒΡΡΩΒΡ «_______________Θ°
Θ®6Θ©‘ΎΜΖΦΚœ©¥÷≤ζΈο’τΝσΙΐ≥Χ÷–Θ§≤ΜΩ…Ρή”ΟΒΫΒΡ“«Τς”–______Θ®Χν’ΐ»Ζ¥πΑΗ±ξΚ≈Θ©Θ°
AΘ°’τΝσ…’ΤΩ BΘ°Έ¬Ε»ΦΤ CΘ°Έϋ¬ΥΤΩ DΘ°άδΡΐΙή EΘ°Ϋ” ’Τς
Θ®7Θ©±Ψ Β―ιΥυΒΟΒΫΒΡΜΖΦΚœ©≤ζ¬ «________Θ®Χν’ΐ»Ζ¥πΑΗ±ξΚ≈Θ©Θ°
AΘ°41% BΘ°50% CΘ°61% DΘ°70%