题目内容
14.在25℃时,某溶液中,由水电离出的c(H+)=1×10-12mol/L,则该溶液的pH可能是2或12.分析 在25℃时,某溶液中,由水电离出的c(H+)水=1.0×10-12 mol/L<10-7mol/L,说明该溶液中的溶质抑制水的电离,溶质能电离出氢离子、氢氧根离子就能抑制水电离,据此分析判断.
解答 解:25℃时:Kw=c(OH-)×c(H+)=10-14,纯水中c(H+)=c(OH-)=1.0×10-7 mol/L,在25℃时,某溶液中,由水电离出的c(H+)水=1.0×10-12 mol/L<10-7mol/L,说明该溶液中的溶质抑制水的电离,溶质能电离出氢离子、氢氧根离子就能抑制水电离,则该溶质可能是酸或碱或强酸的酸式盐,如果为酸溶液,则pH=2,如果为盐溶液,则pH=12,
故答案为:2或12.
点评 本题涉及pH的简单计算,明确溶液中的溶质是抑制水电离是解本题的关键,能电离出氢离子或氢氧根离子的物质抑制水电离,题目难度中等,属于易漏解题.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
4.下列各组气体中,比乙烯含碳量高的是( )
| A. | 甲烷和乙烯 | B. | 乙烷和丁烯 | C. | 乙炔和丙烯 | D. | 乙烯和丁烯 |
2.下列叙述中正确的是( )
| A. | 1 mol任何气体的体积都约为22.4L | |
| B. | 在标准状况下某气体的体积约为22.4L,则该气体约含有6.02×1023个分子 | |
| C. | 16.0gCuSO4•5H2O溶于水配成1L溶液,其物质的量浓度为1mol/L | |
| D. | 标准状况下,22.4LHCl气体溶于1L水中,所得溶液浓度为1mol/L |
9.某有机物的结构简式为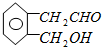 ( )
( )
①加成 ②水解 ③酯化 ④消去.
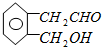 ( )
( )①加成 ②水解 ③酯化 ④消去.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
6.下列酒类,其中酒精含量最高的是( )
| A. | 啤酒 | B. | 白酒 | C. | 葡萄酒 | D. | 黄酒 |
3.如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )
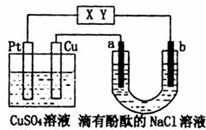

| A. | X极是电源负极,Y极是电源正极 | |
| B. | Pt极上有6.4gCu析出时,b极产生2.24L(标准状况)气体 | |
| C. | a极的电极反应式为:2C1--2e-═C12↑ | |
| D. | 电解过程中 CuSO4溶液的pH逐渐增大 |
10.化学与生产、生活息息相关,下列叙述错误的是( )
| A. | 用聚乙烯塑料代替聚乳酸塑料可减少白色污染 | |
| B. | 含重金属离子的电镀废液不能随意排放 | |
| C. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| D. | Si3N4是一种新型无机非金属材料,可应用于制造发动机 |