题目内容
 水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)═CO (g)+H2 (g)△H=+131.3kJ?mol-1
(1)该反应的平衡常数K随温度的升高而
增大
增大
(增大/减小/不变).(2)上述反应达到平衡后,将体系中的C(s)全部移走,平衡
向左移
向左移
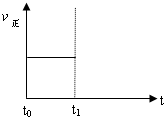
(向左移/向右移/不移动).(3)上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
①缩小容器体积(用实线表示)
②降低温度(用虚线表示)
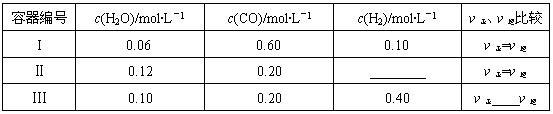
(4)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
| 容器编号 | c(H2O)/mol?L-1 | c(CO)/mol?L-1 | c(H2)/mol?L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | 0.6 0.6 |
ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正 > > ν逆 |
O2+4H++4e-=2H2O
O2+4H++4e-=2H2O
,DMFC的总反应式为2CH3OH+3O2=2CO2+4H2O
2CH3OH+3O2=2CO2+4H2O
.分析:(1)该反应正反应是吸热反应,升高温度平衡向正反应方向移动,据此判断;
(2)将C全部移走,由于是可逆反应,还会生成碳,生成的碳不能完全反应;
(3)①缩小容器体积,压强增大,瞬间正反应速率加快,平衡向逆反应移动,正反应速率增大到新平衡;②降低温度,瞬间正反应速率减慢,平衡逆反应移动,正反应速率增大到新平衡,据此作图;
(4)根据Ⅰ计算平衡常数.Ⅱ中处于平衡状态,根据平衡常数计算Ⅱ中c(H2);
据此Ⅲ中此时的浓度商Qc,与平衡常数比较,判断反应进行的方向,据此判断;
(5)原电池正极发生还原反应,氧气在正极放电,采用质子交换膜,故负极产生的氢离子移向正极,故氧气在正极放电生成水;
该原电池的实质是甲醇燃烧产生二氧化碳与水.
(2)将C全部移走,由于是可逆反应,还会生成碳,生成的碳不能完全反应;
(3)①缩小容器体积,压强增大,瞬间正反应速率加快,平衡向逆反应移动,正反应速率增大到新平衡;②降低温度,瞬间正反应速率减慢,平衡逆反应移动,正反应速率增大到新平衡,据此作图;
(4)根据Ⅰ计算平衡常数.Ⅱ中处于平衡状态,根据平衡常数计算Ⅱ中c(H2);
据此Ⅲ中此时的浓度商Qc,与平衡常数比较,判断反应进行的方向,据此判断;
(5)原电池正极发生还原反应,氧气在正极放电,采用质子交换膜,故负极产生的氢离子移向正极,故氧气在正极放电生成水;
该原电池的实质是甲醇燃烧产生二氧化碳与水.
解答:解:(1)该反应正反应是吸热反应,升高温度平衡向正反应方向移动,平衡常数增大;
故答案为:增大;
(2)将C全部移走,由于是可逆反应,还会生成碳,生成的碳不能完全反应,故平衡向左移动,
故答案为:向左移;
(3)①缩小容器体积,压强增大,瞬间正反应速率加快,平衡向逆反应移动,正反应速率增大到新平衡;②降低温度,瞬间正反应速率减慢,平衡逆反应移动,正反应速率增大到新平衡,故图象为:
故答案为: ;
;
(4)由Ⅰ可知,平衡常数k=
=1,Ⅱ中处于平衡状态,根据平衡常数可知Ⅱ中c(H2)=
=
=0.6,
Ⅲ中此时的浓度商Qc=
=0.8<1,故反应向正反应方向进行,故ν正>ν逆,
故答案为:0.06;>;
(5)原电池正极发生还原反应,氧气在正极放电,采用质子交换膜,故负极产生的氢离子移向正极,故氧气在正极放电生成水,电极反应式为:O2+4H++4e-=2H2O,该原电池的实质是甲醇燃烧产生二氧化碳与水,故总反应式为:2CH3OH+3O2=2CO2+4H2O,
故答案为:O2+4H++4e-=2H2O;2CH3OH+3O2=2CO2+4H2O.
故答案为:增大;
(2)将C全部移走,由于是可逆反应,还会生成碳,生成的碳不能完全反应,故平衡向左移动,
故答案为:向左移;
(3)①缩小容器体积,压强增大,瞬间正反应速率加快,平衡向逆反应移动,正反应速率增大到新平衡;②降低温度,瞬间正反应速率减慢,平衡逆反应移动,正反应速率增大到新平衡,故图象为:

故答案为:
 ;
;(4)由Ⅰ可知,平衡常数k=
| 0.1×0.6 |
| 0.06 |
| K?c(H2O) |
| c(CO) |
| 1×0.12 |
| 0.2 |
Ⅲ中此时的浓度商Qc=
| 0.4×0.2 |
| 0.1 |
故答案为:0.06;>;
(5)原电池正极发生还原反应,氧气在正极放电,采用质子交换膜,故负极产生的氢离子移向正极,故氧气在正极放电生成水,电极反应式为:O2+4H++4e-=2H2O,该原电池的实质是甲醇燃烧产生二氧化碳与水,故总反应式为:2CH3OH+3O2=2CO2+4H2O,
故答案为:O2+4H++4e-=2H2O;2CH3OH+3O2=2CO2+4H2O.
点评:本题考查化学平衡常数及有关计算、化学平衡及反应速率的影响因素、原电池等,难度中等,(2)为易错点、难度,学生容易形成定式思维,认为碳是固体,不影响平衡移动,导致错误,注意审题是将碳完全移走.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g) △H = +131.3 kJ•mol-1
CO (g) +H2 (g) △H = +131.3 kJ•mol-1
(1)该反应的平衡常数K随温度的升高而___________(增大 / 减小 / 不变)。
 (2)上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
(2)上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
① 缩小容器体积(用实线表示)
② 降低温度(用虚线表示)
(3)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器编号 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ________ | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正____ν逆 |
(4)己知:2C (s) + O2(g) = 2CO (g) △H = -221.0 kJ·mo1-1
2CO(g) + O2(g) = 2CO2 (g) △H = -566.0 kJ·mo1-1
2H2 (g) + O2 (g) = 2H2O (g) △H = -483.6 kJ·mo1-1
若将24g炭完全转化为水煤气,然后再充分燃烧,整个过程的焓变为△H = kJ/mol。
水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s)+H2O(g)═CO (g)+H2 (g)△H=+131.3kJ?mol-1
(1)该反应的平衡常数K随温度的升高而______(增大/减小/不变).
(2)上述反应达到平衡后,将体系中的C(s)全部移走,平衡______(向左移/向右移/不移动).
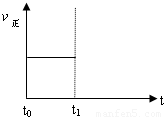
(3)上述反应在t时刻达到平衡(如图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
①缩小容器体积(用实线表示)
②降低温度(用虚线表示)
(4)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
(5)CO和H2可合成甲醇.直接甲醇燃料电池(DMFC)由甲醇负极、氧正极和质子交换膜构成.在催化剂作用下甲醇被氧化为水和二氧化碳.甲醇用完后,只要补充甲醇就可以继续使用.因此,DMFC用作笔记本电脑、汽车等的能量来源时,它能够实现污染物的“零排放”. DMFC的正极电极反应式为______,DMFC的总反应式为______.
C (s)+H2O(g)═CO (g)+H2 (g)△H=+131.3kJ?mol-1
(1)该反应的平衡常数K随温度的升高而______(增大/减小/不变).
(2)上述反应达到平衡后,将体系中的C(s)全部移走,平衡______(向左移/向右移/不移动).
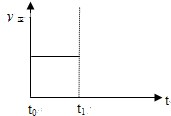
(3)上述反应在t时刻达到平衡(如图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
①缩小容器体积(用实线表示)
②降低温度(用虚线表示)
(4)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
| 容器编号 | c(H2O)/mol?L-1 | c(CO)/mol?L-1 | c(H2)/mol?L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ______ | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正______ν逆 |

 (2009?广州模拟)水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
(2009?广州模拟)水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得: CO (g) +H2 (g) △H= +131.3 kJ?mol-1(······①
CO (g) +H2 (g) △H= +131.3 kJ?mol-1(······①