题目内容
(共8分) A、B、C、D、E是短周期元素,周期表中A与B、B与C相邻;A与E的最外层电子数之比为2:3,B的最外层电子数比E的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红。
(1) E的元素符号是__________。
(2)A、B、C的氢化物稳定性由强到弱的顺序为(用分子式表示)__________________;B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z的晶体类型为____________;用电子式表示AE2的形成过程________________________。
(3)由A、B、C、D、E中的一种或几种元素组成的物质来检验Fe3+的离子方程式为__________________________。
【答案】
(1) S。 (2) H2O>NH3>CH4;
离子晶体;  ∶+
∶+ C
C +∶
+∶

 ∶
∶ C
C ∶
∶
(3)Fe3++3SCN-= Fe(SCN)3。
【解析】常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红,可知C为氧、D为钠。周期表中A与B、B与C相邻;A与E的最外层电子数之比为2:3,可以知道A为碳 B为氮 C为氧 E为硫。三价铁离子用 KSCN检验。

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
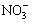 、S
、S 、Cl—、C
、Cl—、C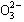 的某一种。
的某一种。