题目内容
工业上常利用CO与SO2反应生成固态S单质和CO2,从而消除这两种气体对大气的污染:2CO(g)+SO2(g) 2CO2(g)+S(s) ΔH=-a kJ/mol(a>0),下列叙述正确的是
2CO2(g)+S(s) ΔH=-a kJ/mol(a>0),下列叙述正确的是
A. 该反应的平衡常数表达式为
B. 若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ
C. 增大压强或升高温度都可以加快化学反应速率并提高SO2的转化率
D. 若单位时间内生成2 mol CO2,同时消耗1 mol SO2,则说明反应达到平衡状态
练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目


 -)>c(H+)
-)>c(H+) 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是 同时,有6个N-H键断裂
同时,有6个N-H键断裂 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
 2CO2+N2。某温度时,在1L密闭容器中充入0.1molCO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率v(NO)=________。若此温度下,某时刻测得CO、NO、N2、CO2的浓度分别为0.01mol/L、amol/L、0.01mol/L、0.04mol/L,要使反应向正反应方向进行,a的取值范围为_____________。
2CO2+N2。某温度时,在1L密闭容器中充入0.1molCO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率v(NO)=________。若此温度下,某时刻测得CO、NO、N2、CO2的浓度分别为0.01mol/L、amol/L、0.01mol/L、0.04mol/L,要使反应向正反应方向进行,a的取值范围为_____________。
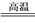 Si3N4+12HCl,有关该反应说法正确的是
Si3N4+12HCl,有关该反应说法正确的是