题目内容
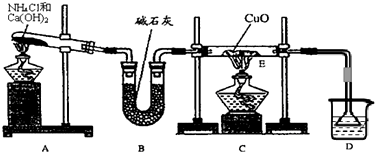
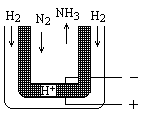
氨是最重要的氮肥原料。在课本里学到的合成氨技术叫哈伯法,近一个世纪,合成氨需要高温高压似乎是天经地义了。然而,最近有两位希腊化学家在《科学》杂志上发表文章说,在常压下把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池(如图),氢气和氮气便可在电极上合成氨,转化率竟然高达78%。
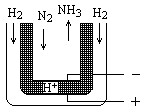
请根据以上材料回答下列问题:
(1)写出哈伯法合成氨的化学方程式: ;其反应条件中,符合平衡移动原理的反应条件是
(2)新法合成氨的电解池中能否用水溶液作电解质? (填“能”、“不能”)
为什么?
(3)电解池中,阳极发生 (填得或失)电子氧化反应,变价元素化合价 (填升高或降低)
(4)新法合成氨中所用的电解质(如图中黑细点所示)能传导H+,试写出电极反应式和总反应式。阳极: ;阴极___________________________
总反应式:__________________________________。
(13分)
(1)(3分,其中方程式2分)N2 + 3H2 ![]() 2NH3 高压
2NH3 高压
(2)(2分) 不能, 此时水不是液态;
(3)(2分) 失 升高
(4)(6分)阳极:3H2 – 6e- == 6H+ (注:生成的H+通过电解质传导到阴极),
阴极:N2 + 6H+ + 6e- == 2NH3
总反应:N2 + 3H2 ![]() 2NH3
2NH3

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目