题目内容
下列变化可用同一原理解释的是
| A.氯水和SO2可使品红褪色 |
| B.浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| C.氯水和活性炭使红墨水褪色 |
| D.氢氧化钠溶液和石灰水暴露在空气中变质 |
D
解析试题分析:A、氯水使品红褪色是因为氯水中的次氯酸具有强氧化性,二氧化硫使品红褪色是因为二氧化硫具有漂白性,原理不同,错误;B、浓硫酸和浓盐酸长期暴露在空气中浓度降低,前者是吸水而使浓度降低,后者是易挥发溶质减少而使浓度降低,原理不同,错误;C、氯水使红墨水褪色是次氯酸的强氧化性,活性炭使红墨水褪色是活性炭的吸附作用,原理不同,错误;D、氢氧化钠溶液和石灰水暴露在空气中变质都是与空气中的二氧化碳反应而变质,原理相同,正确,答案选D,
考点:考查物质的化学变化原理

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
根据下列实验现象得出的结论正确的是
| 选项 | 实验现象 | 结论 |
| A | 将BaSO4浸泡在宝盒Na2CO3溶液中,部分BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| B | 某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定存在SO42- |
| C | 滴有酚酞的Na2CO3溶液中加入BaCl2固体,红色变浅 | Na2CO3溶液中存在水解平衡 |
| D | 溴水中通入SO2,溴水褪色 | SO2具有漂白性 |
对于实验I?IV的描述正确的是
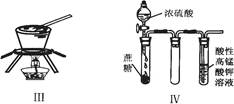
| A.实验I :逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
| B.实验II:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C.实验III:从饱和食盐水中提取NaCl晶体 |
| D.装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内的气体是( )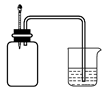
①H2、O2②Cl2、CH4③NO2、O2④N2、H2
| A.①②③ | B.②④ | C.③④ | D.②③ |
下列化学实验事实及其解释都正确的是( )
| A.向KMnO4溶液中滴加盐酸,KMnO4溶液的氧化能力增强。说明盐酸具有氧化性 |
| B.向澄清的AlCl3稀溶液中加入NaOH浓溶液,振荡,溶液仍为澄清。说明该两种溶液混合是物理变化 |
| C.向FeCl3溶液中加入过量Cu粉,振荡、静置,溶液由黄色变为绿色。说明Fe3+具有氧化性 |
| D.向CaCl2溶液中通入CO2,不产生白色沉淀。说明CaCO3能溶于水 |
海洋中有丰富的食品、矿产、能源、药物和水产资源。下图是从海水中提取某些原料的流程图。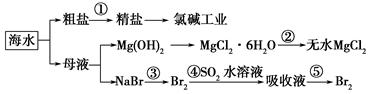
下列有关说法正确的是( )。
| A.第①步中除去粗盐中的SO42—、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液―→NaOH溶液―→BaCl2溶液―→过滤后加盐酸 |
| B.工业上通过氯碱工业制取金属钠 |
| C.从第③步到第⑤步的目的是浓缩、富集溴单质 |
| D.第②步的反应条件是高温加热 |
下列关于海水知识的叙述中不正确的是( )
| A.海水资源的利用包括海水水资源的利用和海水化学资源的利用 |
| B.海水既苦又涩,不能直接利用 |
| C.海水中某些金属元素总储量大,但富集程度却很低 |
| D.海水淡化应同化工生产、能源技术结合 |
下列说法中正确的是( )
| A.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B.青铜是我国使用最早的合金,钢是用量最大、用途最广泛的合金 |
| C.漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂 |
| D.合成纤维和光导纤维都是高分子化合物 |

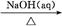 NaAlO2(aq)
NaAlO2(aq)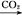 Al(OH)3
Al(OH)3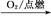 SO3
SO3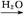 H2SO4
H2SO4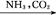 NaHCO3
NaHCO3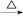 Na2CO3
Na2CO3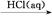 FeCl3(aq)
FeCl3(aq)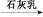 Mg(OH)2
Mg(OH)2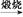 MgO
MgO