题目内容
【题目】某同学在实验报告中记录下列数据,其中正确的是
A. 用 25mL 量筒量取 12.36mL 盐酸
B. 用托盘天平称量 8.75g 食盐
C. 用 500mL 的容量瓶配制 450mL 溶液
D. 用 50mL 蒸馏烧瓶盛装 40mL 溶液进行蒸馏实验
【答案】C
【解析】
A项、量筒应保留小数点后一位有效数字,无法量取12.36mL盐酸,故A错误;
B项、托盘天平的精确度为0.1 g,无法称量8.75g食盐,故B错误;
C.容量瓶的规格和所配制的溶液的体积相符,没有450mL的容量瓶,配制450mL溶液只能用500mL的容量瓶,故C正确;
D项、进行蒸馏实验时,蒸馏烧瓶中的溶液不能超过容器体积的三分之二,故D错误。
故选C。

【题目】已知,常温下H2S、H2CO3 的电离常数如下表
Ka1 | Ka2 | |
H2S | 9.1×10-8 | 1×10-15 |
H2CO3 | 4.3×10-7 | 5.6×10-11 |
(1)①常温下,0.1mol/L的硫化钠溶液和0.1mol.L-1的碳酸钠溶液,碱性更强的是_______。其原因是_____________________________。
② 常温下,硫化钠水解的离子方程式_____________________________。
(2)H2S能与许多金属离子发生反应,生成溶解度不同和各种颜色的金属硫化物沉淀,可用于分离和鉴定金属离子。
①常温下,NaHS溶液显______(选填“酸性”、“中性”或“碱性”)
②常温下,向100 mL 0.1 mol·L-1 H2S溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
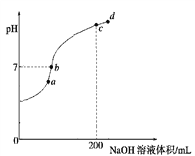
试分析图中a、b、c、d四个点,水的电离程度最大的是________;在b点,溶液中各离子浓度由大到小的排列顺序是______________________________。
(3)脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源,该部分硫化氢用过量NaOH溶液吸收后,再以石墨作电极电解该溶液可回收硫,写出电解得到硫的总反应方程式(忽略氧的氧化还原)_______________;从整个生产工艺的角度分析,该方法不仅能减少环境污染、回收硫、得到一定量的副产物,还具有的优点是___________。