题目内容
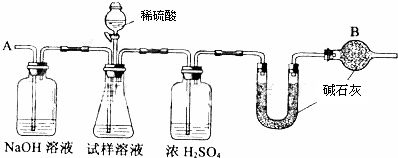
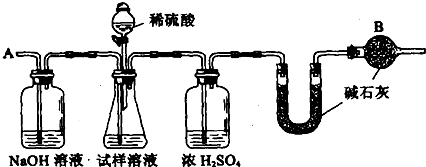
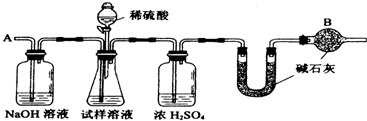
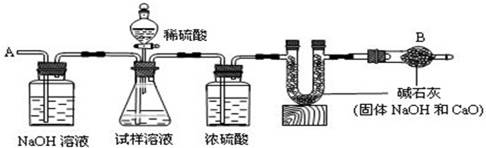
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用图中的装置进行实验。
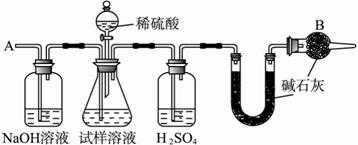
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量,得到b g
④从分液漏斗滴入6 mol?L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,得到c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请填空和完成下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明 。
(2)装置中干燥管B的作用是 。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填“偏高”“偏低”或“不变”)。
(4)步骤⑤的目的是 。
(5)步骤⑦的目的是 。
(6)该试样中纯碱的质量分数的计算式为 。
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
(1)样品重,砝码轻
(2)防止空气中的CO2和水汽进入U形管中
(3)偏高
(4)把反应产生的CO2全部导入U形管中
(5)判断反应产生的CO2是否全部排出,并被U形管中的碱石灰吸收
(6)![]() ×100%
×100%
(7)答案略。
解析:测定方案:①直接测定Na2CO3;可使CO![]() 沉淀,由CaCO3的质量计算Na2CO3的质量。
沉淀,由CaCO3的质量计算Na2CO3的质量。
②测定NaCl的质量;可使Cl-变为AgCl沉淀,由M(AgCl)计算M(NaCl)。
③差量法:可利用Na2CO3与HCl反应的质量差计算Na2CO3的质量。

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目