题目内容
(11分)根据提供条件推断元素,并按要求填空:
1.原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式 ________ ,最高价氧化物对应水化物化学式 ________ ,其最高价氧化物对应水化物与NaOH反应的化学方程式为 ___________________________。
2.第3周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式为______________,最高价氧化物对应水化物与氢氧化钠反应的化学方程式为_______________。
3.原子序数依次递增的同周期四种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为 _______ 、 ________ 、 ________ 、 ________ 。
4.某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧质量分数为60%。则该元素最高价氧化物的化学式为 ________ 。
1. Cl2O7;HClO4;HClO4+ NaOH =NaClO4 + H2O;
2.Al2O3;Al(OH)3 + OH- =[Al(OH)4]-
3.SiH4;PH3;H2S;HCl;
4.SO3;。
解析:考查元素周期表的结构以及常见化学用语的书先。
1.根据已知信息可判断该元素位于第三周期第ⅦA,所以是Cl元素,最高价是+7价。因此最高价氧化物是Cl2O7, 对应水化物化学式HClO4,高氯酸属于强酸和氢氧化钠发生中和反应,方程式为HClO4+ NaOH = NaClO4 +H2O。
2.第3周期元素中最外层电子数与电子层数相同,说明最外层有3个电子,属于原子序数是13,是铝元素。最高价是+3价,因此最高价氧化物的化学式为Al2O3,对应的水化物的化学式为Al(OH)3。氢氧化铝是两性氢氧化物,能溶于强碱氢氧化钠中,方程式为Al(OH)3 + OH- = [Al(OH)4]-。
3.Ar的质子数和电子数都是18,所以这四种元素应该位于第三周期,分别为Si、P、S、Cl,其氢化物分别为SiH4、PH3、H2S、HCl。
4.最高正价与最低负价的代数和为4元素一定属于第ⅥA,最高价是+6价,属于最高价氧化物的化学式为RO3(R表示该元素的元素符号)。根据题意可知 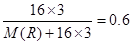 ,解得M(R)=32,因此是硫元素。
,解得M(R)=32,因此是硫元素。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案