题目内容
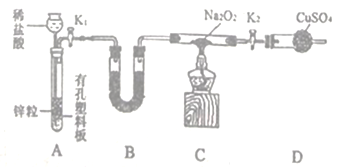
【题目】(1)依据氧化还原反应2Ag+(ag)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

电极X的材料是_______;电解质溶液Y是_________________;银电极为电池的________极,发生的电极反应为______________________;X电极上发生的电极反应为______________________。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为氢氧燃料电池,

写出A电极反应式:___________________________________;写出B电极反应式:_______________________;写出该电池反应:__________。
【答案】铜(或Cu) AgNO3溶液 正 Ag++e-=Ag Cu-2e-=Cu2+ CH4+10OH--8e-=CO32-+7H2O 2O2+8e-+4H2O═8OH- CH4+2O2+2OH-═CO32-+3H2O
【解析】
(1)根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,则Ag为正极,据此分析解答;
(2)甲烷燃料电池中通入CH4的电极为负极,通入氧气的电极为正极,据此分析解答。
(1)根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,电极反应为Cu-2e-=Cu2+,选择硫酸铜为电解质,则Ag为正极,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,应该选用AgNO3为电解质溶液,故答案为:铜(或Cu);AgNO3溶液;正;Ag++e-=Ag;Cu-2e-=Cu2+;
(2)通入CH4的一极为负极,发生氧化反应,在碱性溶液中生成碳酸盐,电极反应为:CH4+10OH--8e-=CO32- +7H2O,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为:2O2+8e-+4H2O═8OH-,电池的总反应为CH4+2O2+2OH-═CO32- +3H2O,故答案为:CH4+10OH--8e-=CO32-+7H2O;2O2+8e-+4H2O═8OH-;CH4+2O2+2OH-═CO32-+3H2O。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案