题目内容
某白色粉末可能含有K2SO4、NH4Cl、NaCl.请设计合理实验探究该白色粉末的组成.限选实验仪器与试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、1mol?L-1硫酸、1mol?L-1硝酸、1mol?L-1盐酸、2mol?L-1NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水.
完成以下实验探究过程:
(1)提出假设:
根据题意,该白色粉末的组成有______种可能的情况.
(2)对于由K2SO4、NH4Cl、NaCl粉末分别配成的溶液,下列说法正确的是______
A.0.1mol/LNH4Cl溶液中的c(NH4+)=c(Cl-)
B.向0.1mol/LNaCl溶液中滴加硝酸,使溶液pH=5,此时混合液中的c(Na+)=c(Cl-)
C.向NH4Cl溶液中加入适量氨水,使混合液的pH=7,此时混合液中c(NH4+)=c(Cl-)
D.在K2SO4溶液中,C(K+)+C(H+)=c(OH-)+c(SO42-)
(3)设计实验方案
基于该粉末中上述三种盐均存在这一假设,设计出实验方案(不要在答题卡上作答).
(4)根据(3)的实验方案,叙述实验操作、预期现象和结论.
| 实验操作 | 预期现象和结论 |
| 步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管. | ______ |
| 步骤2:______ | ______ |
| 步骤3:______ | ______ |
| 步骤4:______ | ______ |
| … |
【答案】分析:(1)K2SO4、NH4Cl、NaCl都是白色粉末药品,该白色粉末的组成有:①K2SO4②NH4Cl③NaCl④K2SO4、NH4Cl⑤NH4Cl、NaCl⑥K2SO4、NaCl⑦K2SO4、NH4Cl、NaCl等7中情况;
(2)从溶液中的盐是否水解和溶液电中性来考虑;
(3)根据三种盐的性质来设计实验步骤;
(4)加热时分解,NH4Cl可观察到现象,向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,NH4Cl的检验也可用NaOH溶液和红色石蕊试纸;充分振荡后静置有白色沉淀生成,证明原白色粉末含有 K2SO4;取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸,有白色沉淀生成,证明原白色粉末含有NaCl.
解答:解:(1)K2SO4、NH4Cl、NaCl都是白色粉末药品,该白色粉末的组成有:①K2SO4②NH4Cl③NaCl④K2SO4、NH4Cl⑤NH4Cl、NaCl⑥K2SO4、NaCl⑦K2SO4、NH4Cl、NaCl等7中情况,故故答案为:7;
(2)A、NH4Cl水解,溶液中的离子浓度应为c(NH4+)<c(Cl-),故A错;
B、NaCl为强酸强碱盐,LNaCl溶液中滴加硝酸,使溶液pH=5,此时混合液中的c(Na+)=c(Cl-),故B正确;
C、根据溶液的电中性原理,向NH4Cl溶液中加入适量氨水,使混合液的pH=7,则,c(H+)=c(OH-),此时混合液中c(NH4+)=c(Cl-);故C正确;
D、根据溶液呈电中性,则有在K2SO4溶液中,C(K+)+C(H+)=c(OH-)+2c(SO42-),故D错.
故答案为:B C;
(3)根据三种盐的性质不同,加热时氯化铵分解,硫酸钡和氯化银都难溶于水来设计实验方案,故答案为:
步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管.
步骤2:用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡.
步骤3:试管B中滴加过量的Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置
步骤4:取试管B中上层清液少量于试管C中,滴加AgNO3溶液和1mol?L-1硝酸
(4)加热时分解,NH4Cl可观察到现象,向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,NH4Cl的检验也可用NaOH溶液和红色石蕊试纸;充分振荡后静置.有白色沉淀生成,证明原白色粉末含有 K2SO4;取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸,有白色沉淀生成,证明原白色粉末含有NaCl.故答案为:
点评:常见元素及化合物的性质,常见离子的检验,常见仪器的使用,提出假设并设计实验方案的能力,学生在遇到不确定因素多的问题时常常抓不住关键,无法理清思路.这也是考纲中要求的“将实际问题分解,通过运用相关知识,采用分析、综合的方法,解决简单化学问题的能力“,即为将总问题分解成若干分问题,逐一解决然后再综合分析.本题的最大障碍是氯化钠的检验这一分问题的解决,要用到的知识大多数学生都是熟悉的,所以不能有效利用的原因是缺乏一种正确的思路:干扰不能轻易排除的情况下必须对物质进行分离,然后再检验.
(2)从溶液中的盐是否水解和溶液电中性来考虑;
(3)根据三种盐的性质来设计实验步骤;
(4)加热时分解,NH4Cl可观察到现象,向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,NH4Cl的检验也可用NaOH溶液和红色石蕊试纸;充分振荡后静置有白色沉淀生成,证明原白色粉末含有 K2SO4;取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸,有白色沉淀生成,证明原白色粉末含有NaCl.
解答:解:(1)K2SO4、NH4Cl、NaCl都是白色粉末药品,该白色粉末的组成有:①K2SO4②NH4Cl③NaCl④K2SO4、NH4Cl⑤NH4Cl、NaCl⑥K2SO4、NaCl⑦K2SO4、NH4Cl、NaCl等7中情况,故故答案为:7;
(2)A、NH4Cl水解,溶液中的离子浓度应为c(NH4+)<c(Cl-),故A错;
B、NaCl为强酸强碱盐,LNaCl溶液中滴加硝酸,使溶液pH=5,此时混合液中的c(Na+)=c(Cl-),故B正确;
C、根据溶液的电中性原理,向NH4Cl溶液中加入适量氨水,使混合液的pH=7,则,c(H+)=c(OH-),此时混合液中c(NH4+)=c(Cl-);故C正确;
D、根据溶液呈电中性,则有在K2SO4溶液中,C(K+)+C(H+)=c(OH-)+2c(SO42-),故D错.
故答案为:B C;
(3)根据三种盐的性质不同,加热时氯化铵分解,硫酸钡和氯化银都难溶于水来设计实验方案,故答案为:
步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管.
步骤2:用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡.
步骤3:试管B中滴加过量的Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置
步骤4:取试管B中上层清液少量于试管C中,滴加AgNO3溶液和1mol?L-1硝酸
(4)加热时分解,NH4Cl可观察到现象,向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,NH4Cl的检验也可用NaOH溶液和红色石蕊试纸;充分振荡后静置.有白色沉淀生成,证明原白色粉末含有 K2SO4;取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸,有白色沉淀生成,证明原白色粉末含有NaCl.故答案为:
| 实验操作 | 预期现象和结论 |
| 白色粉末减少,有白烟生成,试管上部有白色固体凝结,说明原白色粉末含有NH4Cl. | |
| 步骤2:用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡. | 固体溶解得无色溶液. |
| 步骤3:向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置. | 有白色沉淀生成,证明原白色粉末含有 K2SO4. |
| 步骤4:取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸. | 有白色沉淀生成,证明原白色粉末含有NaCl. |
点评:常见元素及化合物的性质,常见离子的检验,常见仪器的使用,提出假设并设计实验方案的能力,学生在遇到不确定因素多的问题时常常抓不住关键,无法理清思路.这也是考纲中要求的“将实际问题分解,通过运用相关知识,采用分析、综合的方法,解决简单化学问题的能力“,即为将总问题分解成若干分问题,逐一解决然后再综合分析.本题的最大障碍是氯化钠的检验这一分问题的解决,要用到的知识大多数学生都是熟悉的,所以不能有效利用的原因是缺乏一种正确的思路:干扰不能轻易排除的情况下必须对物质进行分离,然后再检验.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某白色粉末可能含有K2SO4、NH4Cl、NaCl.请设计合理实验探究该白色粉末的组成.
限选实验仪器与试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、1mol?L-1硫酸、1mol?L-1硝酸、1mol?L-1盐酸、2mol?L-1NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水.
完成以下实验探究过程:
(1)提出假设:
根据题意,该白色粉末的组成有______种可能的情况.
(2)对于由K2SO4、NH4Cl、NaCl粉末分别配成的溶液,下列说法正确的是______
A.0.1mol/LNH4Cl溶液中的c(NH4+)=c(Cl-)
B.向0.1mol/LNaCl溶液中滴加硝酸,使溶液pH=5,此时混合液中的c(Na+)=c(Cl-)
C.向NH4Cl溶液中加入适量氨水,使混合液的pH=7,此时混合液中c(NH4+)=c(Cl-)
D.在K2SO4溶液中,C(K+)+C(H+)=c(OH-)+c(SO42-)
(3)设计实验方案
基于该粉末中上述三种盐均存在这一假设,设计出实验方案(不要在答题卡上作答).
(4)根据(3)的实验方案,叙述实验操作、预期现象和结论.
| 实验操作 | 预期现象和结论 |
| 步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管. | ______ |
| 步骤2:______ | ______ |
| 步骤3:______ | ______ |
| 步骤4:______ | ______ |
| … |
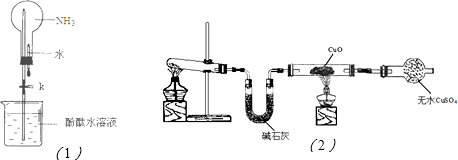
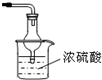 ;
;