题目内容
【题目】已知25℃时,RSO4(s)+CO32-(aq)RCO3(s)+SO42-(aq)的平衡常数K=1.75×104,Ksp(RCO3)=2.80×10-9,下列叙述中正确的是
A.25℃ 时,RSO4的Ksp约为4.9×10-5
B.将浓度均为6×10-5mol/L的RCl2、Na2CO3溶液等体积混合后可得到RCO3沉淀
C.向c(CO32-)=c(SO42-)的混合液中滴加RCl2溶液,首先析出RSO4沉淀
D.相同温度下,RCO3在水中的Ksp大于在Na2CO3溶液中的Ksp
【答案】A
【解析】
25℃时,RSO4(s)+CO32-(aq)RCO3(s)+SO42-(aq)的平衡常数K=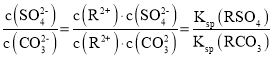 =1.75×104,
=1.75×104,![]() =
=![]() 。
。
A. 根据上述计算分析,25℃ 时,RSO4的Ksp约为4.9×10-5,故A正确;
B. 将浓度均为6×10-5mol/L的RCl2、Na2CO3溶液等体积混合,则浓度变为原来的一半,混合后溶液中c(R2+)=3×10-5mol/L,c(CO32-)=3×10-5mol/L,Qc(RCO3)= c(R2+) c(CO32-)=3×10-5mol/L×3×10-5mol/L=9×10-10< Ksp(RCO3)=2.80×10-9,不会产生RCO3沉淀,故B错误;
C. RSO4、RCO3属于同类型且Ksp(RSO4) > Ksp(RCO3),向c(CO32-)=c(SO42-)的混合液中滴加RCl2溶液,首先析出RCO3沉淀,故C错误;
D. Ksp只与温度有关,与浓度无关,相同温度下RCO3在水中的Ksp等于在Na2CO3溶液中的Ksp,故D错误;
答案选A。

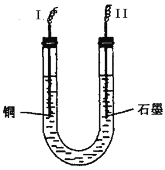
【题目】某同学用如图所示做水果电池的实验,测得数据如下表所示:
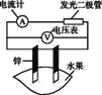
试验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
1 | 锌 | 铜 | 菠萝 | 3 | 900 |
2 | 锌 | 铜 | 苹果 | 3 | 650 |
3 | 锌 | 铜 | 柑桔 | 3 | 850 |
4 | 锌 | 铜 | 西红柿 | 3 | 750 |
5 | 锌 | 铝 | 菠萝 | 3 | 650 |
6 | 锌 | 铝 | 苹果 | 3 | 450 |
请回答以下问题:
(1)实验6中负极的电极反应式为____。
(2)实验1、5中电流方向相反的原因是____。
(3)影响水果电池电压的因素有_____、____。
(4)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做____。(填“合理”或“不合理”)
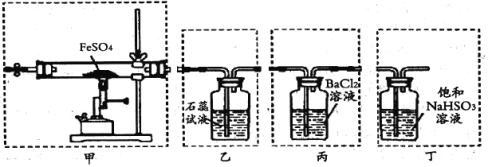
【题目】如图量一套检验气体性质的实验装置。向装置中缓缓通入气体X,若关闭活塞K,则品红溶液褪色。据此判断气体X和洗气瓶内的溶液Y可能的组合是 ( )

A | B | C | D | |
X | 硫化氢 | 二氧化硫 | 二氧化碳 | 氯化氢 |
Y | 浓硫酸 | 饱和NaHCO3 | Na2SO3溶液 | 饱和NaHCO3 |
A.AB.BC.CD.D