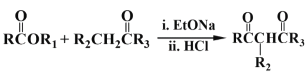题目内容
【题目】反应N2+3H2![]() 2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
A.v(NH3)=0.1mol/(L·s)B.v(N2)=1.0mol/(L·min)
C.v(H2)=1.67mol/(L·min)D.v(H2)=0.3mol/(L·min)
【答案】D
【解析】
根据v=△c÷△t计算v(NH3),再根据速率之比等于化学计量数之比计算v(N2),v(H2)。
v(NH3)=0.6mol·L-1÷3min=0.2mol·(L·min)-1,
速率之比等于化学计量数之比,所以
v(N2)=![]() v(NH3)=
v(NH3)=![]() ×0.2mol·(L·min)-1=0.1mol·(L·min)-1,
×0.2mol·(L·min)-1=0.1mol·(L·min)-1,
v(H2)=![]() v(NH3)=
v(NH3)=![]() ×0.2mol·(L·min)-1=0.3mol·(L·min)-1,
×0.2mol·(L·min)-1=0.3mol·(L·min)-1,
所以ABC错误,D正确;
答案选D。

练习册系列答案
相关题目
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应