题目内容
(10分)高炉炼铁中发生的基本反应之一:FeO(s)+CO(g) Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。
Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值 ,平衡常数K值 (均选填“增大”“减小”或“不变”)。
(2)1 100 ℃时测得高炉中[CO2]="0.025" mol·L-1,[CO]="0.1" mol·L-1,在这种情况下,该反应是否处于化学平衡状态 (选填“是”或“否”),此时,化学反应速率v(正) v(逆)(填“大于”“小于”或“等于”),其原因是 。
 Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。
Fe(s)+CO2(g)(正反应为吸热反应),其平衡常数可表达为K=[CO2]/[CO],已知,1 100 ℃时,K=0.263。(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值 ,平衡常数K值 (均选填“增大”“减小”或“不变”)。
(2)1 100 ℃时测得高炉中[CO2]="0.025" mol·L-1,[CO]="0.1" mol·L-1,在这种情况下,该反应是否处于化学平衡状态 (选填“是”或“否”),此时,化学反应速率v(正) v(逆)(填“大于”“小于”或“等于”),其原因是 。
(1)增大 增大
(2)否 大于 此时[CO2]/[CO]<0.263,因温度不变,K值不变,为增大[CO2]/[CO]比值,平衡需正方向移动〔v(正)>v(逆)〕
(2)否 大于 此时[CO2]/[CO]<0.263,因温度不变,K值不变,为增大[CO2]/[CO]比值,平衡需正方向移动〔v(正)>v(逆)〕
(1)主要考查勒夏特列原理及其应用。升高温度,平衡右移,[CO2]增大,[CO]减小。

练习册系列答案
相关题目
 (填“一定增大”、“一定减小”或“不能确定”)。
(填“一定增大”、“一定减小”或“不能确定”)。 2SO3(g)
2SO3(g) 2SO3;ΔH<0,此时活塞已保持静止,SO2反应速率为v0。再往A内迅速充入2 mol SO2和1 mol O2,当活塞再次保持静止时,SO2反应速率为v,在此过程中,下列说法正确的是
2SO3;ΔH<0,此时活塞已保持静止,SO2反应速率为v0。再往A内迅速充入2 mol SO2和1 mol O2,当活塞再次保持静止时,SO2反应速率为v,在此过程中,下列说法正确的是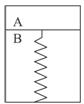
 Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是( )
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是( )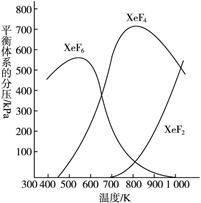
 XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。
XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。 C(g)
C(g) 2NH3。下列有关说法正确的是( )
2NH3。下列有关说法正确的是( ) FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
FeO(s) + CO(g),其温度与平衡常数K的关系如下表: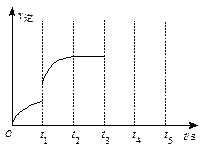
 画出t3~ t5时间段的v逆变化曲线。
画出t3~ t5时间段的v逆变化曲线。