题目内容
在标准状况下进行下列实验:甲、乙、丙各取 0.3 L同浓度的盐酸,加入不同质量的同一镁铝合金粉末,有关数据如下:
甲:合金质量0. 51 g,生成气体体积0.56L;
乙:合金质量0. 765 g,生成气体体积0.672L;
丙:合金质量0. 918 g,生成气体体积0.672L。
求:合金中镁铝的物质的量之比。
甲:合金质量0. 51 g,生成气体体积0.56L;
乙:合金质量0. 765 g,生成气体体积0.672L;
丙:合金质量0. 918 g,生成气体体积0.672L。
求:合金中镁铝的物质的量之比。
解:(1)分析甲、乙、丙三组实验的数据记录:加入合金的质量:m(甲)<m(乙)<m(丙),生成气体的体积:v(甲)v(乙)= v(丙),由于盐酸的体积相同、浓度相同,因此,丙组实验中盐酸不足,甲组实验中盐酸过量。比较甲、乙两组数据:m(甲): m(乙)=1:1.5,V(甲):V(乙)=1:1:2,则乙组实验中盐酸是不足的。盐酸全部反应。
(2)甲组实验中,镁、铝合金完全参加反应,依据合金的质量和产生H2的体积,可以计算合金中镁、铝的物质的量。
设:合金中镁、铝的物质的量分别为x、y。
(2)甲组实验中,镁、铝合金完全参加反应,依据合金的质量和产生H2的体积,可以计算合金中镁、铝的物质的量。
设:合金中镁、铝的物质的量分别为x、y。
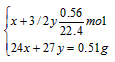
x=y=0. 01mol 则;镁、铝的物质的量之比为1:1。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在标准状况下进行下列实验:甲、乙、丙各取300 mL同浓
度的盐酸,加入不同质量的同一镁铝合金粉末,有关数据列表如下:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 510 | 765 | 918 |
气体体积/mL | 560 | 672 | 672 |
问:(1)盐酸的物质的量浓度是多少?
(2)求合金中镁、铝的质量分数。
(3)在丙实验之后,还需向容器中加入1.00 mol·L-1的NaOH溶液多少毫升才能使剩余合金中的铝全部溶解(设剩余合金与原合金成分相同)?
在标准状况下进行下列实验:甲、乙、丙各取100mL同浓度的盐酸,加入同一镁、铝合金,产生气体,测得有关数据列表如下:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量 | 0.390g | 0.702g | 0.936g |
| 气体体积 | 448mL | 672mL | 672mL |
分析上表数据后计算:
(1) 盐酸的物质的量浓度
(2)合金中镁与铝的物质的量之比
(3)在实验甲反应后溶液中加入过量 0.2mol·L-1的NaOH溶液,欲使生成的沉淀最少,至少应加入多少毫升0.2mol·L-1的NaOH溶液?
在标准状况下进行下列实验:甲、乙、丙各取100mL同浓度的盐酸,加入同一镁、铝合金,产生气体,测得有关数据列表如下:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量 | 0.390g | 0.702g | 0.936g |
| 气体体积 | 448mL | 672mL | 672mL |
(1)盐酸的物质的量浓度
(2)合金中镁与铝的物质的量之比
(3)在实验甲反应后溶液中加入过量 0.
 2mol·L-1的NaOH溶液,欲使生成的沉淀最少,至少应加入多少毫升0.2mol·L-1的NaOH溶液?
2mol·L-1的NaOH溶液,欲使生成的沉淀最少,至少应加入多少毫升0.2mol·L-1的NaOH溶液? 在标准状况下进行下列实验:甲、乙、丙各取100mL同浓度的盐酸,加入同一镁、铝合金,产生气体,测得有关数据列表如下:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量 |
0.390g |
0.702g |
0.936g |
|
气体体积 |
448mL |
672mL |
672mL |
分析上表数据后计算:
(1) 盐酸的物质的量浓度
(2)合金中镁与铝的物质的量之比
(3)在实验甲反应后溶液中加入过量 0.2mol·L-1的NaOH溶液,欲使生成的沉淀最少,至少应加入多少毫升0.2mol·L-1的NaOH溶液?