题目内容
5.有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环.其中一种合成路线如图: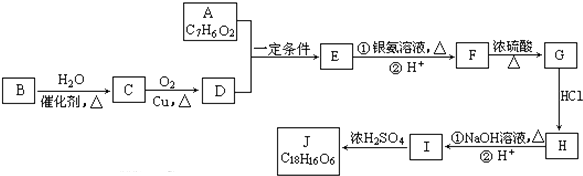
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1:2:2:1.
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平.
③R1-CHO+R2-CH-CH2O$\stackrel{一定条件}{→}$
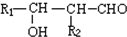
回答以下问题:
(1)A中含有的官能团名称是羟基和醛基.
(2)写出有机反应类型B→C加成反应,I→J取代反应(或酯化反应).
(3)写出F生成G的化学方程式
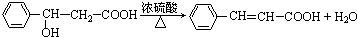 .
.(4)写出J的结构简式
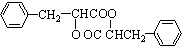 .
.(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式
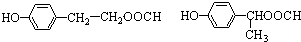 .
.①FeCl3溶液发生显色反应 ②能发生银镜反应
③苯环上只有两个对位取代基 ④能发生水解反应.
分析 有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平,则B为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生氧化反应得D为CH3CHO,A既能发生银镜反应,又能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,其核磁共振氢谱显示有4种氢,且峰面积之比为1:2:2:1,根据A的分子式可知,A为 ,A与D发生题中信息中的反应生成E为
,A与D发生题中信息中的反应生成E为 ,E发生氧化反应生成F为
,E发生氧化反应生成F为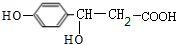 ,F在浓硫酸作用下发生消去反应生成G为
,F在浓硫酸作用下发生消去反应生成G为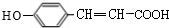 ,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为
,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为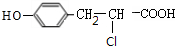 ,H在碱性条件下发生水解生成I为
,H在碱性条件下发生水解生成I为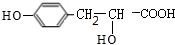 ,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为
,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为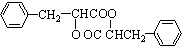 ,据此答题.
,据此答题.
解答 解:有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平,则B为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生氧化反应得D为CH3CHO,A既能发生银镜反应,又能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,其核磁共振氢谱显示有4种氢,且峰面积之比为1:2:2:1,根据A的分子式可知,A为 ,A与D发生题中信息中的反应生成E为
,A与D发生题中信息中的反应生成E为 ,E发生氧化反应生成F为
,E发生氧化反应生成F为 ,F在浓硫酸作用下发生消去反应生成G为
,F在浓硫酸作用下发生消去反应生成G为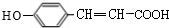 ,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为
,根据J分子结构中含有3个六元环可知,G与氯化氢发生加成反应,氯原子加在羧基邻位碳上,生成H为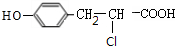 ,H在碱性条件下发生水解生成I为
,H在碱性条件下发生水解生成I为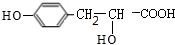 ,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为
,两分子I在浓硫酸作用下发生成酯化反应,生成环酯J为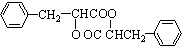 ,
,
(1)A为 ,A中含有的官能团名称是羟基和醛基,
,A中含有的官能团名称是羟基和醛基,
故答案为:羟基和醛基;
(2)根据上面的分析可知,B→C为加成反应,I→J为取代反应(或酯化反应),
故答案为:加成反应;取代反应(或酯化反应);
(3)F生成G的化学方程式为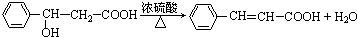 ,
,
故答案为: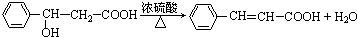 ;
;
(4)根据上面的分析可知,J的结构简式为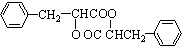 ,
,
故答案为: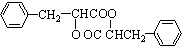 ;
;
(5)E的同分异构体,符合以下要求①FeCl3溶液发生显色反应,说明有酚羟基,②能发生银镜反应,说明有醛基,③苯环上只有两个对位取代基 ④能发生水解反应,说明有酯基,则符合条件的E的同分异构体的结构简式为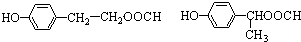 ,
,
故答案为: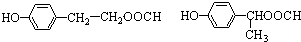 .
.
点评 本题考查有机物的合成,明确合成路线中各物质的推断是解答本题的关键,注意碳链骨架、官能团的变化、反应条件与反应类型的关系即可解答,题目难度中等.

| A. | 高锰酸钾 | B. | 生理盐水 | C. | 空气 | D. | 大理石 |
| A. | H2O2、H2O | B. | Cl2和氯水 | C. | 氧气和液氧 | D. | 白磷和红磷 |
| A. | 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其生腐蚀 | |
| B. | 反应SO2(g)+2H2S(g)=3S(S)+2H2O(l)在常温下能自发进行,则该反应的△H<0 | |
| C. | 0.1mol•L-1的CH3COOH溶液加水稀释,溶液的pH和溶液中水的电离程度均增大 | |
| D. | 常温下,将等体积、等物质的量浓度的NaHCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得溶液pH<7,存在KW/c(H+)>1.0×10-7 mol•L-1 |
| A. | 用渗析的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| B. | 用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2杂质 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| A. | 13、1 | B. | 13、2 | C. | 11、1 | D. | 10、2 |
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | CO2+H2O═H2CO3 | ||
| C. | Fe+H2SO4=FeSO4+H2↑ | D. | MgCO3+2HCl═2HCl2+CO2↑+H2O |

