题目内容
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)===I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是
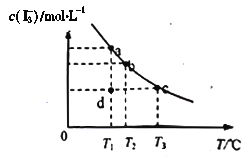
A. 温度为T1时,向该平衡体系中加入KI固体,平衡正向移动
B. 反应I2(aq)+I-(aq)===I3-(aq) △H<0
C. 若T1时,反应进行到状态d时,一定有v正>v逆
D. 状态a与状态b相比,状态b时I2的转化率更高
【答案】D
【解析】A、温度T1时,加入KI固体,碘离子浓度增大,升高温度平衡向正反应方向移动,故A正确;B、由图象曲线的变化趋势可知,当温度升高时,I3-的物质的量浓度减小,说明该反应的正反应为放热反应,反应I2(aq)+I-(aq)I3-(aq)的△H<0,故B正确;C、若反应进行到状态d时,反应未达到平衡状态,若反应趋向于平衡,则反应向生成的I3-方向移动,则v正>v逆,故C正确;D、状态b相当于在状态a的基础上升高温度,该反应的正反应为放热反应,升高温度,平衡向逆反应方向移动,状态b时I2的转化率更低,故D错误;故选D。

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目