题目内容
|
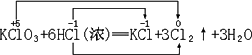
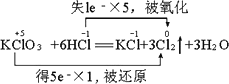
在反应KClO3+6HCl(浓) | |
A. |
6∶1 |
B. |
5∶1 |
C. |
1∶5 |
D. |
1∶6 |
答案:B
解析:
解析:
|
解析:根据化合价的高变高,低变低规律有:
根据电子守恒得:
当有5 mol电子发生转移时,被氧化的氯原子与被还原的氯原子的物质的量之比为5∶1. 思路导引:根据高变高、低变低规律制定 Cl元素化合价的变化;根据电子守恒,判定被氧化和被还原的Cl原子个数比. |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目