题目内容
有A、B、C、D、E5种元素,已知:
① A原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子第三层上的电子比第一层多5个。
② 常温下B2是气体,它对氢气的相对密度是16。
③ C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④ D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1) A是________、B是________、C是________、D是________、E是________。(写元素符号)
(2) E的原子结构示意图为________________,C的离子结构示意图为________________。
(3) F和AB2反应的化学方程式为 。
(1)碳、氧、钠、硫、氯
(2)Cl , Na+
, Na+ 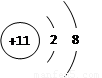 2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
【解析】
试题分析:A原子最外层电子数是次外层电子数的两倍,所以根据核外电子的排布规律可知,A的质子数应该是2+4=6,即A是碳元素;常温下B2是气体,它对氢气的相对密度是16,所以该单质的相对分子质量是16×2=32,又因为B的阴离子与C的阳离子跟氖原子的电子层结构相同,所以B是氧元素;C的单质在B2中燃烧,生成淡黄色固体F,因此C是钠,则F是过氧化钠;D在DB2中的含量为50%,所以D的相对原子质量是32。又因为D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,所以D应该是S元素;E原子第三层上的电子比第一层多5个,所以E的质子数是2+8+7=17,即E是氯元素。
考点:考查元素周期表的结构及核外电子排布规律的应用
点评:该题属于典型的高考题型,为中等难度的试题。本题比较全面考查学生有关元素知识的推断,有利于培养学生的答题能力和综合应用基础知识解决实际问题的能力。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案




