题目内容
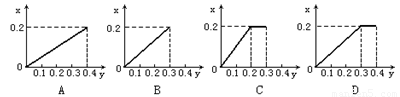
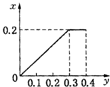
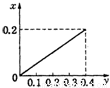
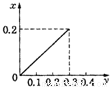
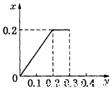
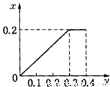
将22.4g铁粉逐渐加入到含HNO3 0.8mol的稀硝酸中,反应生成的气体的物质的量(x)随消耗铁粉的物质的量(y)变化关系中正确的是( )A.
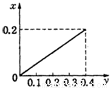
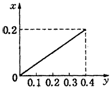
B.
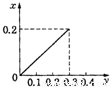
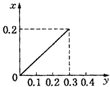
C.
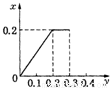
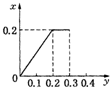
D.
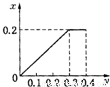
【答案】分析:铁粉逐渐加入到含HNO3 0.8mol的稀硝酸中,开始硝酸过量,铁与硝酸反应生成硝酸铁、一氧化氮,当硝酸反应完毕后,铁若有剩余,再与硝酸铁反应生成硝酸亚铁.
先判断铁与硝酸反应生成硝酸铁、一氧化氮,铁是否有剩余,若铁有剩余根据硝酸计算生成NO的物质的量,若硝酸有剩余根据铁计算生成NO的物质的量.
解答:解:22.4g铁的物质的量为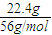 =0.4mol,令铁完全反应需硝酸的物质的量为n,则:
=0.4mol,令铁完全反应需硝酸的物质的量为n,则:
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+H2
1 4
0.4mol n
所以n=1.6mol,由于1.6mol>0.8mol,所以Fe有剩余,根据硝酸计算生成NO的物质的量,参加反应生成NO的Fe的物质的量,则:
Fe+4HNO3(稀)=Fe(NO3)3 +NO↑+H2
1mol 4 mol 0.1mol
0.2mol 0.8mol 0.2mol
根据生成NO的物质的量,参加反应生成NO的Fe的物质的量作图,反应生成的气体的物质的量(x)随消耗铁粉的物质的量(y)变化关系如图:
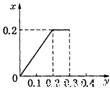
故选:C.
点评:考查硝酸的性质、过量计算,难度中等,注意铁粉逐渐加入到稀硝酸中,开始硝酸过量,铁与硝酸反应生成硝酸铁.
先判断铁与硝酸反应生成硝酸铁、一氧化氮,铁是否有剩余,若铁有剩余根据硝酸计算生成NO的物质的量,若硝酸有剩余根据铁计算生成NO的物质的量.
解答:解:22.4g铁的物质的量为
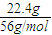 =0.4mol,令铁完全反应需硝酸的物质的量为n,则:
=0.4mol,令铁完全反应需硝酸的物质的量为n,则:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+H2
1 4
0.4mol n
所以n=1.6mol,由于1.6mol>0.8mol,所以Fe有剩余,根据硝酸计算生成NO的物质的量,参加反应生成NO的Fe的物质的量,则:
Fe+4HNO3(稀)=Fe(NO3)3 +NO↑+H2
1mol 4 mol 0.1mol
0.2mol 0.8mol 0.2mol
根据生成NO的物质的量,参加反应生成NO的Fe的物质的量作图,反应生成的气体的物质的量(x)随消耗铁粉的物质的量(y)变化关系如图:

故选:C.
点评:考查硝酸的性质、过量计算,难度中等,注意铁粉逐渐加入到稀硝酸中,开始硝酸过量,铁与硝酸反应生成硝酸铁.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目