题目内容
13.根据元素周期表和周期律分析下面推断错误的是( )| A. | 铍原子失电子能力比镁弱 | B. | HI比HAt稳定 | ||
| C. | 氢氧化铝碱性比氢氧化镁强 | D. | 高氯酸的酸性比硫酸强 |
分析 A、铍和镁均位于第ⅡA族,铍位于第二周期,镁位于第三周期,同一主族从上到下金属性逐渐增强,失电子能力增强,故铍原子失电子能力比镁弱;
B、碘和砹均位于同一主族,碘位于第五周期,砹位于第六周期,从上到下非金属逐渐减弱;
C、铝的金属性比镁弱,金属性越强,最高价氧化物对应水化物的碱性增强;
D、非金属性越强,最高价氧化物对应水化物的酸性越强.
解答 解:A、铍和镁均位于第ⅡA族,铍位于第二周期,镁位于第三周期,同一主族从上到下金属性逐渐增强,失电子能力增强,故铍原子失电子能力比镁弱,故A正确;
B、碘和砹均位于同一主族,碘位于第五周期,砹位于第六周期,从上到下非金属逐渐减弱,砹的氢化物不如碘化氢稳定,故B正确;
C、铝的金属性比镁弱,金属性越强,最高价氧化物对应水化物的碱性增强,所以氢氧化铝碱性比氢氧化镁弱,故C错误;
D、非金属性越强,最高价氧化物对应水化物的酸性越强,而氯的非金属性强于硫,所以高氯酸的酸性比硫酸强,故D正确;
故选C.
点评 本题考查了同主族元素性质的相似性和递变性,利用相似性和递变性来推断已知常见元素与不常见元素性质的递变性.

练习册系列答案
相关题目
3.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素B的原子最外层电子数是其电子层数的3倍,元素A的价电子数比B少2,元素D与A同主族,元素C与E形成的化合物CE是厨房常用调味品:下列说法正确的是( )
| A. | C和E的单质可通过电解饱和的CE水溶液获得 | |
| B. | 原子半径:C>D>A>B | |
| C. | A、D、E的最高价氧化物对应水化物的酸性逐渐增强 | |
| D. | C与B形成的两种化合物中化学键类型完全相同 |
4.下列各项中表达正确的是( )
| A. | Si的原子结构示意图: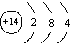 | |
| B. | 聚乙烯的结构简式 | |
| C. | 原子核内有20个中子的氯原子:${\;}_{37}^{17}$Cl | |
| D. | HCl的电子式: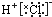 |
18.1mL密度为0.93g•cm-3的氨水恰好中和0.005mol H2SO4生成(NH4)2SO4,若要配制上述浓度的氨水,在1L水中需要溶解标准状况下的氨气( )
| A. | 294.7L | B. | 378.0L | C. | 2240.0L | D. | 1120.0L |

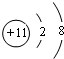 ,它的最高价氧化物对应水化物中含有的化学键有离子键、(极性)共价键,工业上冶炼D单质的化学方程式为2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑.
,它的最高价氧化物对应水化物中含有的化学键有离子键、(极性)共价键,工业上冶炼D单质的化学方程式为2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑. .
. ④
④ ⑤
⑤ ⑥
⑥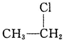 ⑦
⑦
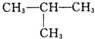 ⑨CH3-CH═CH2(10)CH3-CO-CH3 (11)
⑨CH3-CH═CH2(10)CH3-CO-CH3 (11) (12)
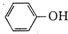
(12)
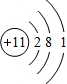
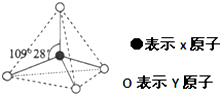 现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同.单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.
现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同.单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.