题目内容
(14分)实验室用固体烧碱配制500mL 1 mol/L的NaOH溶液
(1)(4分)需称量 g的烧碱固体,固体应放在 中称量。
(2)(4分)配制过程中除了烧杯还需要哪些仪器
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低或无影响)(4分)
①定容时俯视刻度线 ②容量瓶未干燥
③转移过程中有少量液体溅出
④未洗涤烧杯和玻璃棒
(4)(2分)若定容时液面高于刻度线应采取的措施是
(1)(4分)需称量 g的烧碱固体,固体应放在 中称量。
(2)(4分)配制过程中除了烧杯还需要哪些仪器
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低或无影响)(4分)
①定容时俯视刻度线 ②容量瓶未干燥
③转移过程中有少量液体溅出
④未洗涤烧杯和玻璃棒
(4)(2分)若定容时液面高于刻度线应采取的措施是
(1)(每空2分)20.0g 小烧杯
(2)(每个1分)托盘天平 玻璃棒 500ml容量瓶 胶头滴管
(3)(每个1分)偏高 无影响 偏低 偏低
(4)2分 重新配制
(2)(每个1分)托盘天平 玻璃棒 500ml容量瓶 胶头滴管
(3)(每个1分)偏高 无影响 偏低 偏低
(4)2分 重新配制
考查一定物质的量浓度的配制。
(1)根据物质的量浓度的概念可知,需要氢氧化钠的物质的量为0.5L×1mol/L=0.5mol,其质量是0.5mol×40g/mol=20.0g.氢氧化钠易潮解,称量时要放在小烧杯中称量。
(2)称量需要托盘天平,溶解需要玻璃棒,定容需要500ml容量瓶和胶头滴管。
(3)①导致容量瓶中的溶液体积偏小,结果偏高。②不影响。③导致溶质的物质的量减少,结果偏低。④导致溶质的物质的量减少,结果偏低。
(4)定容时液面一旦高于刻度线,则结果偏低,即实验已经失败,需要重新配制。
(1)根据物质的量浓度的概念可知,需要氢氧化钠的物质的量为0.5L×1mol/L=0.5mol,其质量是0.5mol×40g/mol=20.0g.氢氧化钠易潮解,称量时要放在小烧杯中称量。
(2)称量需要托盘天平,溶解需要玻璃棒,定容需要500ml容量瓶和胶头滴管。
(3)①导致容量瓶中的溶液体积偏小,结果偏高。②不影响。③导致溶质的物质的量减少,结果偏低。④导致溶质的物质的量减少,结果偏低。
(4)定容时液面一旦高于刻度线,则结果偏低,即实验已经失败,需要重新配制。

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目

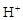 使石蕊变色
使石蕊变色