题目内容
2.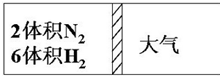 在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通如图所示.容器中发生以下反应:N2+3H2?2NH3(正反应为放热反应).若反应达平衡后,测得混合气体的体积为7体积,据此回答下列问题:
在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通如图所示.容器中发生以下反应:N2+3H2?2NH3(正反应为放热反应).若反应达平衡后,测得混合气体的体积为7体积,据此回答下列问题:(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的体积仍与上述平衡时完全相同,那么:①若a=1,c=2,则b=3.在此情况下,反应起始时将向逆(填“正”或“逆”)反应方向进行.②若需规定起始时反应向逆反应方向进行,则c的范围是1<c≤4.
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是降低温度,原因是6.5<7上述平衡需向气体体积缩小方向移动,故可采取降温措施.
分析 (1)①在恒温恒压下,要使平衡状态与原平衡状态完全等效,可以采用极限转化处理,按化学计量数转化到左边,应满足2体积N2、6体积H2,计算原平衡时氨气的体积,根据氨气体积判断反应进行方向;
②若让反应逆向进行,氨气的体积必须大于原平衡时氨气的体积,最大值则为2体积氮气和6体积氢气完全反应时产生的氨气的体积;
(2)平衡后混合气体为6.5体积<7体积,恒压条件下,应是改变温度影响平衡移动,根据温度对化学平衡移动的影响知识来回答.
解答 解:(1)①反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同,恒温恒压条件下,采用极限分析,按化学计量数转化到左边,应满足2体积N2、6体积H2,2体积的氨气完全转化得到1体积氮气、3体积氢气,故1+a=1+1=2,3+b=6,则b=3,
所以只要a:b=1:3,由于a=1,则b=3,
因反应前混合气体为8体积,反应后混合气体为7体积,体积差为1体积,则:
N2(g)+3H2(g)?2NH3(g) 体积减少
2 2
1体积 1体积
故平衡时氨气为1体积,而在起始时,氨气的体积c=2体积,比平衡状态时大,为达到同一平衡状态,氨的体积必须减小,所以平衡逆向移动,
故答案为:3;逆;
②若让反应逆向进行,由上述①所求出的平衡时氨气为1体积,氨气的体积必须大于1体积,最大值则为2体积氮气和6体积氢气完全反应时产生的氨气的体积,即为4体积,则1<c≤4,
故答案为:1<c≤4;
(2)平衡后混合气体为6.5体积<7体积,恒压条件下,应是改变温度影响平衡移动,由于正反应为放热反应,且是气体总分子数减小的反应,只能为降低温度,
故答案为:降低温度;6.5<7上述平衡需向气体体积缩小方向移动,故可采取降温措施.
点评 本题主要考查了等效平衡、化学平衡影响因素等,注意理解等效平衡原理,注意各物质的量与原平衡相等,按化学计量数转化到左边满足对应物质等量,不能是等比.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案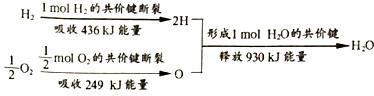
| A. | 分子发生化学变化时,会生成新的分子,但不会分裂成原子 | |
| B. | 2molH2和1molO2完全反应,结果放出930kJ的热量 | |
| C. | 1molH-H和$\frac{1}{2}$molO-O键的断裂过程共放出930KJ的热量 | |
| D. | 分析变化的全过程,可得出形成H-O键将放出能量 |
| A. | 碱性:KOH>NaOH | B. | 溶解度:SO2>CO2 | ||
| C. | 酸性:HClO4>H2SO4 | D. | 气态氢化物的稳定性:H2O>NH3 |

| A. | c (Ag+) | B. | 溶液的pH | C. | Ag棒的质量 | D. | c(NO3-) |
| A. | 分子组成相差一个或若干个CH2原子团的化合物一定互为同系物 | |
| B. | 互为同分异构体的有机物的组成元素相同,但结构必须不同 | |
| C. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| D. | 互为同系物的有机物其相对分子质量数值一定相差14n(n为正整数) |
| A. | 直线 sp杂化 | B. | V型 sp杂化 | ||
| C. | 三角锥形 sp2杂化 | D. | 平面三角形 sp2杂化 |
| A. | 将苯滴入溴水中,振荡后水层接近无色 | |
| B. | 乙烯使酸性KMnO4溶液褪色 | |
| C. | 乙烯使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
| A. | 1:2 | B. | 2:1 | C. | 7:8 | D. | 8:7 |
