题目内容
【题目】在密闭容器中进行的反应:N2 + 3H22NH3,下列说法正确的是
A. 降低温度能加快逆反应速率
B. 保持体积不变充入N2,能加快反应速率
C. 达到平衡时,反应速率:v(正) =v(逆)=0
D. 达到平衡时,N2和H2的转化率可能达到100%
【答案】B
【解析】
A.降低温度能减慢化学反应速率,故A错误;
B. 保持体积不变充入N2,增大反应物的浓度,能加快反应速率,故B正确;
C. 化学平衡是动态平衡,达到平衡时,反应速率:v(正)=v(逆)>0,故C错误;
D. 化学平衡研究的对象是可逆反应,可逆反应不可完全转化,所以氮气和氢气不可能完全转化,故D错误。答案选B。

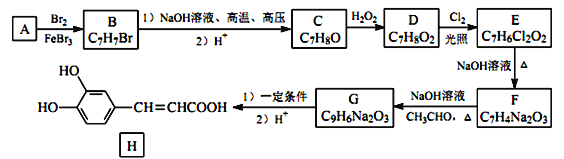
【题目】碳、氮广泛分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s) + 6C(s) + 2N2(g)![]() Si3N4(s) + 6CO(g) ΔH=-1591.2 kJ/mol则该反应每转移1mol e-,可放出的热量为________
Si3N4(s) + 6CO(g) ΔH=-1591.2 kJ/mol则该反应每转移1mol e-,可放出的热量为________
(2)高温时,用CO还原MgSO4可制备高纯MgO
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是:____________
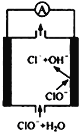
②由MgO制成的Mg可构成“镁—次氯酸盐”电池,其装置示意图如图,该电池的正极反应式为____________
(3)某研究小组将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g) + H2O(g)![]() CO2(g) + H2(g),得到如下数据:
CO2(g) + H2(g),得到如下数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
CO | H2O | CO | H2 | |||
1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
2 | 900 | 1 | 2 | 0.5 | 0.5 | — |
①实验Ⅰ中,前5min的反应速率v(CO2)=___________
②下列能判断实验Ⅱ已经达到平衡状态的是(填写选项序号)__________
a.容器内CO、H2O、CO2、H2的浓度不再变化
b.容器内压强不再变化
c.混合气体的密度保持不变
d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
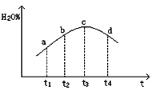
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示,b点v正_______v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是______________________