题目内容
19.下列叙述正确的是( )| A. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| B. | 、SiO2是酸性氧化物,能与NaOH溶液反应 | |
| C. | 、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | .除去石英中的少量碳酸钙,用稀硫酸溶解后过滤分离 |
分析 A、氧化钠与二氧化碳反应生成碳酸钠,二氧化碳与过氧化钠反应生成碳酸钠和氧气;
B、酸性氧化物与碱反应生成盐和水;
C、氮的氧化物都有毒,都是大气污染物,而一氧化氮极易被空气中的氧气氧化成二氧化氮;
D、根据碳酸钙与稀硫酸反应产生硫酸钙,硫酸钙微溶,产生了新杂质.
解答 解:A、氧化钠与二氧化碳反应生成碳酸钠,二氧化碳与过氧化钠反应生成碳酸钠和氧气,二者产物不同,故A错误;
B.SiO2是酸性氧化物,酸性氧化物能与NaOH溶液反应生成盐和水,所以SiO2能与NaOH溶液反应,故B正确;
C.NO能和氧气反应生成二氧化氮,所以在空气中都不能稳定存在,故C错误;
D.碳酸钙与稀硫酸反应产生硫酸钙,硫酸钙微溶,产生了新杂质,不符合除杂原理,故D错误;
故选:B.
点评 本题主要考查了物质的性质以及除杂原理,难度不大,注意知识的积累.

练习册系列答案
相关题目
7.下列叙述正确的是( )
| A. | 物质的量浓度相同的溶液中所含溶质的微粒数相同 | |
| B. | 常温常压下,0.1molH2气体约含6.02×1022个H2分子 | |
| C. | 1mol•L-1醋酸溶液100mL中H+的个数约为0.1NA | |
| D. | 标准状况下,1molH2O的体积约22.4L |
14.已知:
CH3CH2CH2CH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ/mol
下列说法正确的是( )
CH3CH2CH2CH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ/mol
下列说法正确的是( )
| A. | 正丁烷的稳定性大于异丁烷 | |
| B. | 异丁烷分子中的碳氢键比正丁烷的多 | |
| C. | 等物质的量的正丁烷能量大于异丁烷能量 | |
| D. | 异丁烷转化为正丁烷的过程是一个放热过程 |
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标况下,11.2L SO3所含的分子数目为0.5 NA | |
| B. | 1L0.1 mol•L-1的碳酸氢钠溶液中含碳酸氢根离子数为0.1NA | |
| C. | 常温常压下,1.7gH2O2中含有的电子数为0.9nA | |
| D. | 8 Al+3 NH4ClO4═4 Al2O3+3NH3+3HCl 反应中,消耗27gAl粉时,转移的电子数目为2.75NA |
11.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸.当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐.
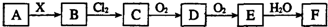
下列说法中不正确的是( )
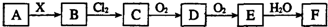
下列说法中不正确的是( )
| A. | 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4 | |
| B. | 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3 | |
| C. | B和Cl2的反应是氧化还原反应 | |
| D. | 当X是强酸时,C在常温下是气态单质 |
8.将12g金属粉末混合物,加入足量稀硫酸中,至无气泡产生为止,共收集到氢气11.2L(标准状况下),此混合物可能是( )
| A. | Zn和Cu | B. | Al和Fe | C. | Ag和Zn | D. | Mg和Fe |
9.NA代表阿伏加德罗常数,下列有关叙述错误的是( )
| A. | 56g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA | |
| B. | 标准状况下22.4升CH4和C2H4的混合气体所含氢原子数为4NA28bNA | |
| C. | 常温常压下,3.4gNH3中含N-H键数目为0.6NA | |
| D. | CO2通过足量Na2O2使固体增重bg时,反应中转移的电子数为$\frac{b{N}_{A}}{2}$ |
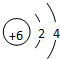 .
.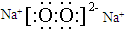 ;如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式AlO2-+CO2+2H2O=Al(OH)3↓+HCO3 -.
;如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式AlO2-+CO2+2H2O=Al(OH)3↓+HCO3 -.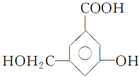
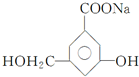 、
、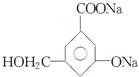 、
、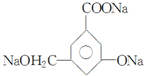 .
.