题目内容
某工厂的工业废水中含有大量的硫酸亚铁、较多的Cu2+和较少的Na+以及部分泥沙.为了减少污染并变废为宝,工厂计划从该废水中回收绿矾和金属铜.请根据如图流程图完成实验方案.
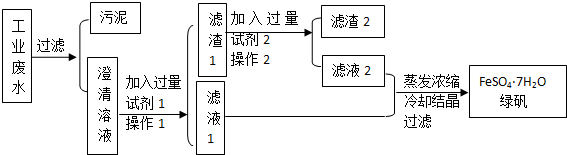
(1)操作1的名称 .
(2)写出加入试剂或药品的名称:试剂1 ,试剂2 .
(3)滤渣2所含物质的化学式为 .
(4)在澄清溶液中加入试剂1后发生化学反应,请写出该反应的离子方程式 .
(5)滤渣1中加入试剂2后发生化学反应,请写出该反应的离子方程式 .

(1)操作1的名称
(2)写出加入试剂或药品的名称:试剂1
(3)滤渣2所含物质的化学式为
(4)在澄清溶液中加入试剂1后发生化学反应,请写出该反应的离子方程式
(5)滤渣1中加入试剂2后发生化学反应,请写出该反应的离子方程式
考点:物质分离、提纯的实验方案设计,物质的分离、提纯的基本方法选择与应用
专题:实验设计题
分析:工业废水中含大量硫酸亚铁、Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,试剂1为Fe,操作I为过滤,试剂2为稀硫酸,操作2为过滤,则滤液2中含硫酸亚铁,滤渣2为Cu,滤液1中含硫酸亚铁,然后蒸发、浓缩、结晶、过滤,可得到FeSO4.7H2O,以此来解答.
解答:
解:工业废水中含大量硫酸亚铁、Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,试剂1为Fe,操作I为过滤,试剂2为稀硫酸,操作2为过滤,则滤液2中含硫酸亚铁,滤渣2为Cu,滤液1中含硫酸亚铁,然后蒸发、浓缩、结晶、过滤,可得到FeSO4.7H2O,
(1)由上述分析可知,操作1为过滤,分离不溶性固体与液体,故答案为:过滤;
(2)由上述分析可知,试剂1为Fe,发生Cu2++Fe=Fe2++Cu,试剂2为硫酸,铁粉、铜中加入适量稀硫酸,稀硫酸和铁粉反应生成硫酸亚铁,故答案为:Fe;稀硫酸;
(3)铁粉、铜中加H2SO4得到FeSO4,Cu不反应,则滤渣2为Cu,故答案为:Cu;
(4)加入试剂1后发生化学反应,其离子反应为Cu2++Fe=Fe2++Cu,故答案为:Cu2++Fe=Fe2++Cu;
(5)加入试剂2后发生化学反应,且离子反应为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑.
(1)由上述分析可知,操作1为过滤,分离不溶性固体与液体,故答案为:过滤;
(2)由上述分析可知,试剂1为Fe,发生Cu2++Fe=Fe2++Cu,试剂2为硫酸,铁粉、铜中加入适量稀硫酸,稀硫酸和铁粉反应生成硫酸亚铁,故答案为:Fe;稀硫酸;
(3)铁粉、铜中加H2SO4得到FeSO4,Cu不反应,则滤渣2为Cu,故答案为:Cu;
(4)加入试剂1后发生化学反应,其离子反应为Cu2++Fe=Fe2++Cu,故答案为:Cu2++Fe=Fe2++Cu;
(5)加入试剂2后发生化学反应,且离子反应为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑.
点评:本题考查混合物分离提纯实验方案的设计,为高频考点,把握实验流程中的试剂及发生的反应、混合物分离方法为解答的关键,侧重分析与推断能力的考查,注意物质的性质、物质之间的反应,题目难度不大.

练习册系列答案
相关题目
下列两种气体的体积一定相等的是( )
| A、质量相等,密度相等的Cl2和NH3 |
| B、同温同质量的CO和C2H4 |
| C、同温同压下同质量的CO2和SO2 |
| D、同压同质量的C3H6和CO2 |
下列离子方程式正确的是( )
| A、向小苏打溶液中加入醋酸溶液:HCO3-+H+=CO2↑+H2O |
| B、氢氧化镁与稀硫酸反应:H++OH-=H2O |
| C、钠与水反应,有氢气产生:Na+H2O=Na++OH-+H2↑ |
| D、碳酸钙与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
反应2NO2(g)?2NO(g)+O2(g);△H>0,密闭容器中进行,并达到平衡.要使体系中气体颜色加深,正反应速率降低,应采用的措施是( )
| A、加压 | B、减压 |
| C、降温 | D、充入氧气 |
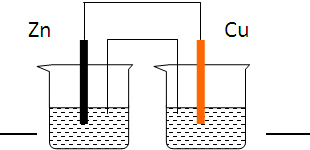 总反应:Zn+Cu2+=Zn2++Cu.
总反应:Zn+Cu2+=Zn2++Cu.