题目内容
)电子表和电子计算器的电池常用微型银—锌原电池,其电极分别为Zn和Ag2O,电解质溶液为KOH溶液,负极反应 和总反应分别为:Zn+2OH - -2e==ZnO+H2O和Ag2O+Zn==ZnO+2Ag
(1)该原电池工作时负极区溶液的PH值 (上升、下降或不变)
(2)该原电池工作时电子由 (Zn或Ag2O)极经外电路流向 (正或负)极。正极上发生的电极反应为
【答案】
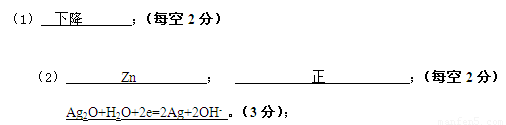
【解析】略

练习册系列答案
相关题目
电子表和电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为一定浓度的KOH溶液,放电时锌极上的电极反应式为:Zn-2e—+2OH—==Zn(OH)2;氧化银电极上的反应式为:Ag2O+2e—+H2O==2Ag+2OH-,总反应式为:Ag2O+H2O+Zn==Zn(OH)2+2Ag。下列说法正确的是
| A.溶液中OH— 向正极移动,K+、H+向负极移动 |
| B.锌发生还原反应,氧化银发生氧化反应 |
| C.锌是负极,氧化银是正极 |
| D.随着电极反应的不断进行,电解质的碱性减弱 |