题目内容
【题目】化合物H可用以下路线合成:

已知:![]()
请回答下列问题:
(1)标准状况下11.2L烃A在氧气中充分燃烧可以生成88gCO2和45gH2O,且A分子结构中有3个甲基,则A的结构简式为________________________;
(2)B和C均为一氯代烃,D的名称(系统命名)为_________________;
(3)在催化剂存在下1molF与2molH2反应,生成3—苯基—1—丙醇。F的结构简式是___________;
(4)反应①的反应类型是_______________________;
(5)反应②的化学方程式为______________________________________;
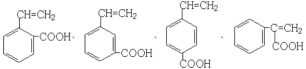
(6)写出所有与G具有相同官能团的芳香类同分异构体的结构简式_______________。
【答案】CH3CH(CH3)CH3 2—甲基丙烯 ![]() 消去反应
消去反应 ![]()
【解析】
(1)88gCO2为2mol,45gH2O为2.5mol,标准状况下11.2L气体物质的量为0.5mol,所以烃A中含碳原子为4,H原子数为10,则化学式为C4H10,因为A分子结构中有3个甲基,则A的结构简式为:CH3CH(CH3)CH3;
(2)C4H10存在正丁烷和异丁烷两种,但从框图上看,A与Cl2光照取代时有两种产物,且在NaOH醇溶液作用下的产物只有一种,则A只能是异丁烷,先取代再消去生成的D名称为:2—甲基丙烯;
(3)F可以与Cu(OH)2反应,故应为醛基,与H2之间为1:2加成,则应含有碳碳双键.从生成的产物3-苯基-1-丙醇分析,F的结构简式为![]() ;
;
(4)反应①为卤代烃在醇溶液中的消去反应,故答案为:消去反应;
(5)F被新制的Cu(OH)2氧化成羧酸G为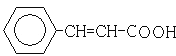 ,D至E为信息相同的条件,则类比可不难得出E的结构为
,D至E为信息相同的条件,则类比可不难得出E的结构为![]() ,E与G在浓硫酸作用下可以发生酯化反应,反应方程式为:
,E与G在浓硫酸作用下可以发生酯化反应,反应方程式为:
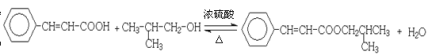 ;
;
(6)G中含有官能团有碳碳双键和羧基,可以将官能团作相应的位置变换而得出其芳香类的同分异构体为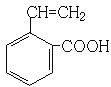 、
、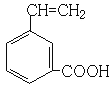 、
、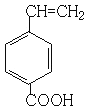 、
、 。
。

 阅读快车系列答案
阅读快车系列答案【题目】Ⅰ、氯化亚铜(CuCl)难溶于水,常用作催化剂、气体吸收剂及脱氯剂等。
(1)向一定比例的CuSO4、NaCl溶液中持续加入一定浓度的Na2SO3溶液可制得CuCl。加入的Na2SO3溶液体积与溶液pH关系如图所示。
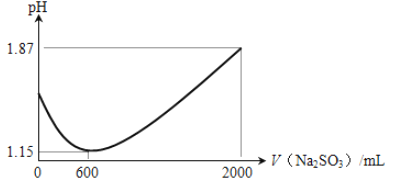
① 0 ~ 600 mL时pH降低的原因是_______(用离子方程式表示);
② 600 ~ 2000 mL的过程中有刺激性气味的气体产生,该气体是__________。
(2)CuCl的另一种制备原理是Cu2++Cu+2Cl-=2CuCl K=5.85×106,向0.01 molL-1的CuCl2溶液中加入足量的铜,写出计算过程说明能否生成CuCl: ________。
(3)使用CuCl捕捉CO气体的反应为CuCl(s) + xCO(g) ![]() CuClxCO(s) △H < 0,为提高CO的平衡转化率,可采取的措施有____(填标号)。
CuClxCO(s) △H < 0,为提高CO的平衡转化率,可采取的措施有____(填标号)。
A.降低温度 B.增大压强
C.延长反应时间 D.把CuCl分散到疏松多孔的分子筛中
Ⅱ、钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1mol/L的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
pH | 8.8 | 9.7 | 11.6 | 10.3 |
上述盐溶液中的阴离子,结合氢离子能力最强的是__________ ;根据表中数据,下列三种酸的溶液分别稀释100倍,pH变化最大的是(填序号)___________
A. HClO B.H2CO3 C. CH3COOH
(2)次氯酸钠是一种 ______(填“强”或“弱”)电解质。某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是______(请用反应的离子方程式表示)。
(3)实验室中常用氢氧化钠来进行洗气和提纯。
当150mL 1mol/L的氢氧化钠溶液吸收标况下2.24L二氧化碳时,所得溶液中各离子浓度由大到小的顺序为:_________。